
2026年2月12日,中国科学院上海营养与健康研究所秦骏、肖意传,复旦大学彭俊杰、华中科技大学王桂华,同济大学林谋斌共同通讯在Cancer Cell(IF=44.5)在线发表题为“Chemotherapy triggers immune evasion by fostering LEPR+ Kupffer cell differentiation in liver metastases”的研究论文。该研究表明化疗通过促进肝转移瘤中LEPR+库普弗细胞分化触发免疫逃避。

该研究团队通过构建多种肝转移瘤小鼠模型,并结合临床样本分析,深入探究了化疗对肝转移瘤免疫微环境的影响。研究发现,化疗药物在杀伤肿瘤细胞的同时,会诱导肝脏中的库普弗细胞向LEPR+(瘦素受体阳性)亚型分化。
(一)动物模型构建与化疗处理
肝转移瘤模型建立:研究团队构建了多种肝转移瘤小鼠模型,包括:
结直肠癌肝转移模型:通过脾脏注射MC38、CT26结肠癌细胞系建立;
黑色素瘤肝转移模型:通过尾静脉注射B16-F10黑色素瘤细胞建立;
乳腺癌肝转移模型:通过尾静脉注射4T1乳腺癌细胞建立。
化疗方案实施:采用临床常用化疗药物奥沙利铂(Oxaliplatin)和5-氟尿嘧啶(5-FU)处理荷瘤小鼠,模拟临床化疗过程。
(二)免疫细胞表型与功能分析
流式细胞术检测:分离小鼠肝脏中的免疫细胞,通过流式细胞术分析化疗前后库普弗细胞(Kupffer Cells, KCs)的表型变化,发现化疗后LEPR+ KCs比例显著升高。
单细胞RNA测序(scRNA-seq):对化疗前后的肝脏KCs进行单细胞转录组测序,鉴定出LEPR+ KCs的特异性基因表达谱,发现其高表达免疫抑制相关基因(如TGF-β、IL-10)和吞噬相关基因(如MerTK)。
(三)LEPR+ KCs功能验证
吞噬功能实验:通过荧光标记的凋亡肿瘤细胞,检测LEPR+ KCs对凋亡细胞的吞噬能力,发现其吞噬能力显著强于普通KCs。
免疫抑制功能实验:将LEPR+ KCs与CD8+ T细胞共培养,检测T细胞的增殖和细胞因子分泌情况,发现LEPR+ KCs可显著抑制CD8+ T细胞的增殖和IFN-γ的分泌。
(四)机制探究实验
ICD分子检测:检测化疗后肿瘤细胞释放的损伤相关分子模式(DAMPs),如ATP、HMGB1等,发现LEPR+ KCs可通过MerTK受体吞噬这些DAMPs分子,从而抑制免疫激活。
信号通路验证:通过敲低或过表达LEPR+ KCs中的关键基因(如MerTK、TGF-β),验证其在免疫逃避中的作用,发现敲低MerTK可恢复肿瘤免疫原性,增强CD8+ T细胞的抗肿瘤活性。
(五)临床样本验证
收集结直肠癌肝转移患者化疗前后的肝组织样本,通过免疫组化和流式细胞术检测LEPR+ KCs的比例和分布,发现化疗后患者肝组织中LEPR+ KCs比例显著升高,且与患者预后不良相关。
核心研究结论
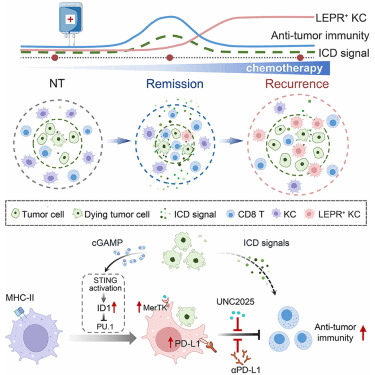
化疗诱导LEPR+ KCs分化:化疗药物可将肝脏中的常规KCs重编程为LEPR+ KCs,这一过程与化疗诱导的肿瘤细胞凋亡及DAMPs释放密切相关。
LEPR+ KCs介导免疫逃避:LEPR+ KCs通过MerTK依赖的吞噬作用清除化疗诱导产生的ICD信号(如ATP、HMGB1),同时分泌免疫抑制因子(如TGF-β、IL-10),抑制CD8+ T细胞的活化和增殖,从而帮助肝转移瘤逃避机体免疫监视。
靶向LEPR+ KCs可逆转耐药:通过抑制MerTK受体或清除LEPR+ KCs,可恢复肿瘤免疫原性,增强CD8+ T细胞的抗肿瘤活性,联合免疫检查点抑制剂(如抗PD-1抗体)可显著提高化疗对肝转移瘤的治疗效果,为临床治疗提供了新的策略。
库普弗细胞
库普弗细胞是肝脏中的固有巨噬细胞,在维持肝脏免疫稳态、清除病原体和肿瘤细胞等方面发挥着重要作用。然而,在化疗的作用下,库普弗细胞的功能发生了显著改变。LEPR+库普弗细胞能够通过多种途径抑制机体的抗肿瘤免疫反应,从而促进肿瘤细胞的免疫逃避。
一方面,LEPR+库普弗细胞可以分泌大量的免疫抑制因子,如转化生长因子-β(TGF-β)、白细胞介素-10(IL-10)等。这些因子能够抑制效应T细胞的增殖和活化,削弱T细胞的抗肿瘤功能。同时,它们还能促进调节性T细胞(Treg)的扩增,进一步加剧免疫抑制微环境的形成。
另一方面,LEPR+库普弗细胞还可以通过表达程序性死亡配体-1(PD-L1)等免疫检查点分子,与T细胞表面的程序性死亡受体-1(PD-1)结合,启动T细胞的凋亡信号通路,导致T细胞耗竭,无法有效杀伤肿瘤细胞。
此外,研究团队还发现,LEPR+库普弗细胞的分化与化疗诱导的肿瘤细胞损伤密切相关。化疗导致肿瘤细胞释放大量的损伤相关分子模式(DAMPs),如高迁移率族蛋白B1(HMGB1)等。这些分子能够激活肝脏中的炎症信号通路,进而诱导库普弗细胞向LEPR+亚型分化。
在恶性肿瘤的治疗进程中,化疗一直占据着核心地位,尤其是对于晚期转移性肿瘤患者,化疗是延长生存期、改善生活质量的重要手段。然而,临床治疗中常常面临着化疗耐药和肿瘤免疫逃避的难题,这严重制约了化疗的疗效,成为肿瘤治疗领域亟待攻克的瓶颈。
肝脏作为恶性肿瘤最常见的转移器官之一,胃癌、结直肠癌、乳腺癌等多种肿瘤都极易发生肝转移。肝转移瘤的治疗难度大,患者预后差,化疗虽然能在一定程度上控制肿瘤进展,但肿瘤细胞往往能通过多种机制逃避机体免疫系统的监视和攻击,导致治疗失败。因此,深入解析肝转移瘤中化疗诱导免疫逃避的分子机制,寻找新的治疗靶点,对于提升肝转移瘤的治疗效果具有重要的临床意义。
治疗抵抗机制
LEPR+库普弗细胞在肝转移瘤中扮演着“变节哨兵”的角色
1起始信号:化疗触发“危险信号”释放
cGAMP:进入库普弗细胞,激活STING信号通路,上调转录因子ID1,抑制PU.1,解除对细胞分化的限制,驱动其向LEPR+表型转化 。
ATP:作为趋化信号,被LEPR+库普弗细胞表面高表达的P2RY2受体识别,引导其从肿瘤边缘向内部浸润 。
2免疫清除屏蔽:吞噬“死亡证据”
LEPR+库普弗细胞具有极强的吞噬能力(胞葬作用),通过表面MerTK受体识别并清除化疗诱导产生的免疫原性细胞死亡(ICD)分子(如CRT、HMGB1等) 。这相当于“打扫战场”,使免疫系统无法感知肿瘤细胞死亡,从而抑制抗肿瘤免疫反应的启动
3免疫微环境重塑:构建抑制性生态
高表达PD-L1,与T细胞的PD-1结合,导致T细胞耗竭 。分泌大量抑制性细胞因子,如TGF-β、IL-10,抑制效应T细胞活性,促进调节性T细胞(Treg)扩增 。
这些变化共同将肝转移灶的免疫微环境从“免疫激活”推向“免疫抑制”状态。
4跨癌种保守性与临床关联
该机制在结直肠癌、黑色素瘤、乳腺癌等多种肝转移模型中均被验证,且在化疗后复发患者中LEPR+库普弗细胞比例显著升高,提示其为共性耐药机制 。
结 语
秦骏、肖意传等团队的这项研究成果深入揭示了化疗诱导肝转移瘤免疫逃避的新机制,为肝转移瘤的治疗提供了重要的理论基础和潜在的治疗靶点。这一研究不仅有助于我们更好地理解肿瘤免疫微环境在化疗耐药中的作用,也为开发新型的肿瘤治疗策略提供了新的思路。
未来,随着研究的不断深入,我们有望进一步阐明LEPR+库普弗细胞在肿瘤发生、发展和转移中的其他作用机制,开发出更加精准、有效的靶向治疗药物。同时,通过开展大规模的临床研究,验证这些治疗策略的安全性和有效性,将研究成果转化为临床实践,为广大肝转移瘤患者带来新的希望。
参考文献
1:https://www.cell.com/cancer-cell/abstract/S1535-6108(26)00049-8
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

