
在全球超10亿人受肥胖困扰的当下,肥胖早已不只是外观问题,更是通往2型糖尿病、心血管疾病乃至癌症的高危通道。人们皆知减肥是破解困局的有效方法,却鲜少知晓体重下降背后,脂肪组织内部正上演着一场关乎细胞衰老与重生的精密革命。2025年7月发表于《Nature》的论文《Selective remodelling of the adipose niche in obesity and weight loss》,首次以高分辨率视角,为我们揭开了减肥如何清扫脂肪组织、逆转细胞衰老的神秘面纱。

研究过程
研究人员对来自极端肥胖男性和女性的约100000个细胞进行了单核RNA测序(n = 25) WL手术前后和健康瘦对照组(n = 24;图1a)。WL显著改善了代谢参数,尽管没有达到瘦基线(图1b和扩展数据表1)。我们关注腹部皮下AT,因为它对中心性肥胖的贡献及其相对于其他皮下AT依赖物的不良代谢影响。研究结果与已发表的最大的人类皮下脂肪图谱中的另外50000个细胞(核)相结合,以改善细胞注释(n = 9 肥胖和n = 4 贫样;扩展数据图1a-c)。等效队列中的空间转录组学(约25000个细胞,n = 4 每组;图1a,扩展数据图1b,c和扩展数据表1)使我们能够在健康和功能失调的AT的组织层次结构中定位和情境化细胞表型
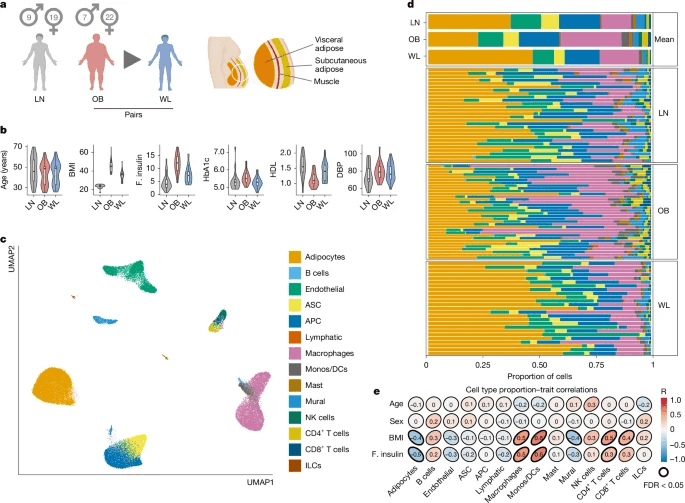
全组织聚类(图1c)和成分分析表明,肥胖AT中存在广泛的免疫细胞(主要是巨噬细胞,但也有淋巴细胞)浸润(图1d,e和扩展数据图1d,e)。肥胖AT也显示出成熟脂肪细胞的缺陷,表明细胞死亡增加和/或未能补充成熟脂肪细胞。WL减轻了这些典型的有害影响。
免疫细胞浸润是肥胖AT7的一个病理特征,但WL对炎症重塑的影响尚不清楚,研究表明具有相反的抗炎和促炎作用。研究聚集了髓系细胞(n = 34,280;图2a,扩展数据图2a和补充表2)分为AT巨噬细胞、单核细胞和树突状细胞(MYE1-10)的异质亚类。
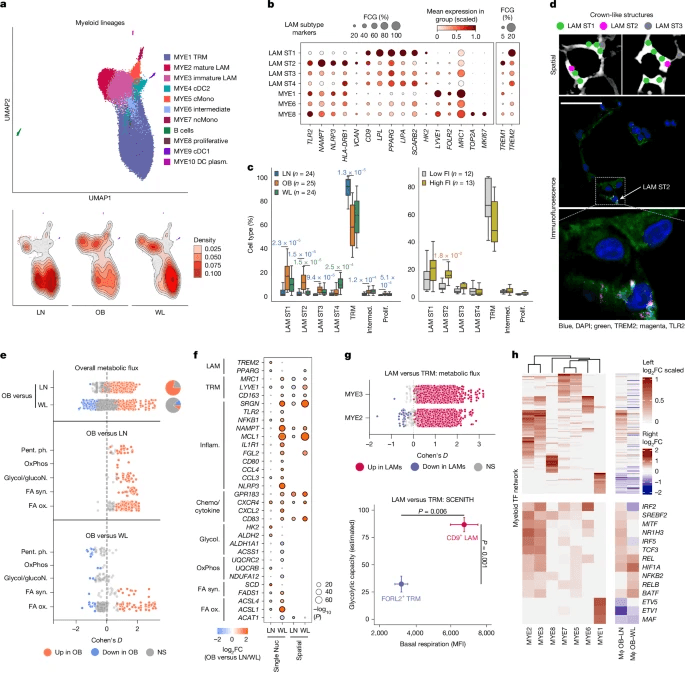
比例分析显示,表达稳态标志物(LYVE1、FOLR2和MRC1;扩展数据图2c)的组织驻留巨噬细胞(MYE1和TRM)比例较低。邻域图证实,这代表了相对(而非绝对)的TRM减少(扩展数据图2b)。增殖的巨噬细胞表达MCP-1(CCL2)、TRM和LAM标志物,支持人类肥胖中这两个群体的低水平MCP-1依赖性扩张(扩展数据图2a)。
肥胖患者的炎症性LAM数量增加,与代谢功能障碍有关(图2c)。空间和蛋白质分析表明,适应性LAM在冠状结构(CLS;转录缺失的脂肪细胞周围)聚集,炎性LAM在分离或成对时更为丰富(图2d和扩展数据图2e-g)。
表明不同的髓系类别在肥胖AT中经历了广泛的代谢启动。实验能量分析证实了LAM比TRM具有更高的基础活性和糖酵解能力,证实了基于转录组的通量结果(图2g和扩展数据图2i)。尽管广泛的WL,肥胖诱导的髓系细胞状态仍然存在。转录组通量分析证实,WL并没有完全逆转全局代谢活化(图2e和扩展数据图3b)
总体数量低(6222个细胞(4%);扩展数据图2l-n)意味着无法评估淋巴亚类水平的变化。然而,肥胖AT的CD4+和CD8+T细胞、NK细胞和B细胞比例较高,WL改善了重塑作用(扩展数据图2n)。WL还下调了淋巴细胞活化和细胞毒性基因(ETS1和SYTL3;补充表7和8),进一步支持炎症减少。
WL导致应激脂肪细胞显著减少(平均从55%减少到14%),纤维化数量减少,脂质生物合成细胞相对增加(图3b)。原位验证了胁迫和脂质生物合成群体的组成变化(扩展数据图4c)。米色脂肪细胞很少见(AD8-GATM-hi,1%),在不同条件下不变。
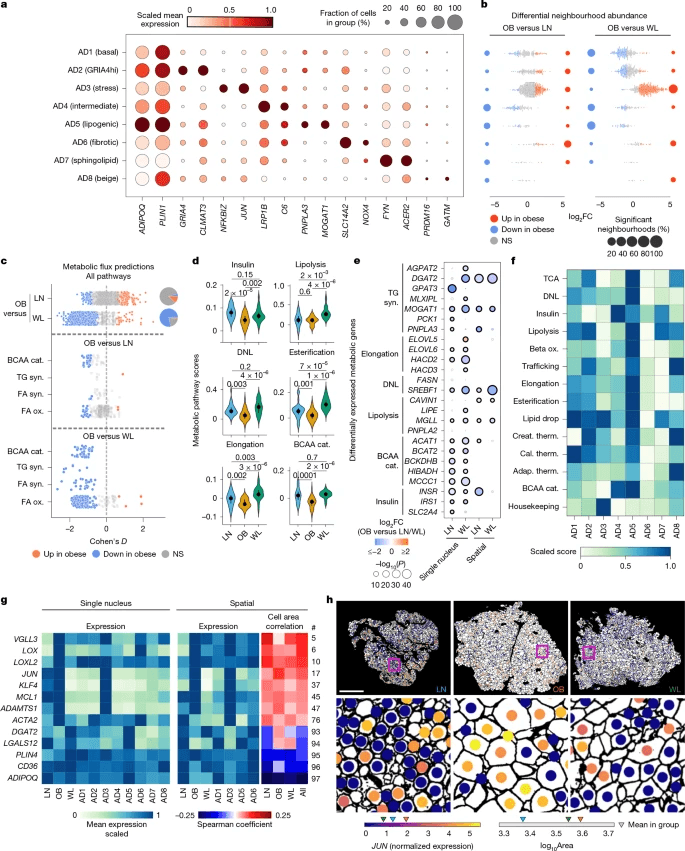
与瘦脂肪细胞相比,肥胖细胞的脂肪酸和支链氨基酸(BCAA)分解存在显著缺陷,这与之前的结果相吻合,共同表明代谢灵活性受损(图3c和扩展数据图3a)。相比之下,WL导致脂肪细胞代谢通量在全球范围内显著增加(1895次反应中有1485次;二项式检验,P = 1.4 × 10−142;图3c,扩展数据图1f和3b以及补充表6)可能反映了负能量平衡。
WL还逆转了BCAA分解代谢中的缺陷(通路通量和典型酶;图3c-e和扩展数据图4f),其预测结果是系统性BCAA清除和改善胰岛素敏感性。脂质循环是PNPLA3在脂肪细胞(AD5)中的一个特征,而应激(AD3)脂肪细胞的特征是代谢周转率较低(图3f)。WL的这些典型的分解代谢和以前未被认识的合成代谢作用表明,底物动员参与了细胞自主循环途径,这可能是代谢稳态广泛改善的基础。
脂肪细胞祖细胞(APCs)再生成熟的脂肪细胞并维持组织基质,这是肥胖可能受损的关键稳态功能。APC分为:“多能”DPP4-CD55-hi祖细胞(ASC/APC1);表达典型分化基因的“承诺”前脂肪细胞(APC2和APC3);脂肪生成调节细胞(APC4、KCNIP-hi和CD142/F3-hi);以及纤维化前体(APC5、ADAM12-hi和POSTN-hi)(扩展数据图5a-c和补充表2)。APC3表现出与成熟脂肪细胞相似的应激特征,以及NOCT的高表达(图4a和扩展数据图5c),NOCT是前脂肪细胞承诺的潜在限制性看门人。
压力和纤维化细胞数量再次反映了肥胖,并随着WL的增加而显著减少(图4b和扩展数据图6a、b)。这两个群体都有较高的缺氧诱导因子1A(HIF1A;图4a和扩展数据图6a,c)表达,其促进小鼠纤维化并抑制脂肪生成(通过PPARG磷酸化)。相应地,WL下调了缺氧、促纤维化(TGFβ)和抗脂肪生成(WNT)基因(扩展数据图6c和补充表7和8)。因此,WL可以减轻某些人类APC亚群中缺氧诱导的分化能力和促纤维化信号的损伤。
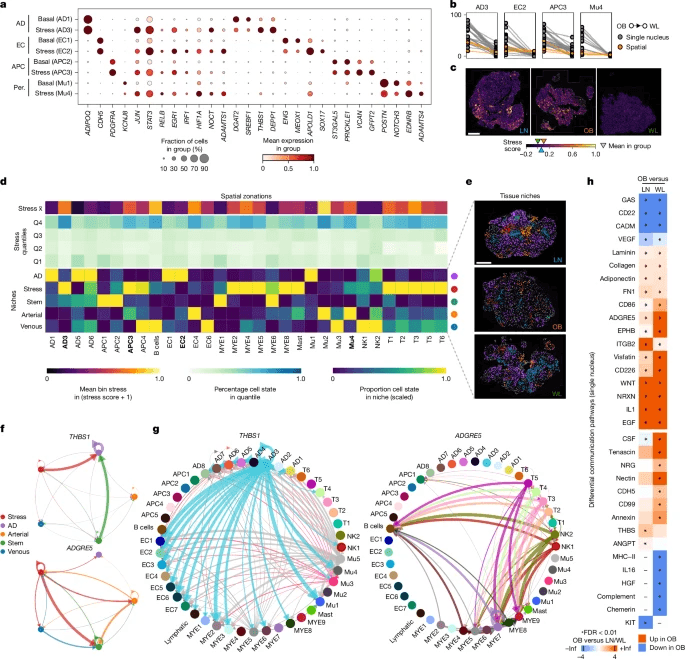
所有受压力的细胞状态都上调了一个共同的基因特征(188个基因;扩展数据图6d、e和补充表12)。多细胞应激虽然在肥胖中最高,但却是瘦组织的一个特征,随着年龄和代谢功能障碍的增加而增加(图4c和扩展数据图6f,g)。基因和通路分析揭示了多细胞应激的假定介质(缺氧、机械和氧化应激、Gp130介导的细胞因子、DNA损伤和细胞周期阻滞;扩展数据图7a,b)。体外诱导DNA损伤(使用依托泊苷)概括了体内对应激标记蛋白和受损ASPC分化能力的影响(扩展数据图7c–e)。WL导致多细胞应激基因显著减少(扩展数据图6c),总体上强调了多细胞应激途径在组织损伤和修复中的重要性。
研究发现,除TRM和NK细胞外,应激区域与免疫细胞之间存在很强的关联,并且与动脉内皮细胞之间存在意想不到的联系(EC4;图4d)。这确定了五个不同的细胞群落,称为动脉、静脉、脂肪细胞、干细胞和应激生态位(图4d、e和扩展数据图8c)
为了并证实了对不同衰老特征的抑制(图5a和扩展数据图10a)。在多种细胞类型中,WL导致CDKN1A(p21)的下调,CDKN1A是衰老过程中主要的细胞周期抑制剂之一,并导致p21抑制的细胞周期进展基因的上调。相应地,WL显著降低了主要衰老标志物的表达和无偏衰老评分(图5a和扩展数据图10a-d)。我们发现p21阳性细胞具有衰老细胞的转录特征(扩展数据图10e),在应激脂肪细胞、前体细胞和血管细胞状态中最为普遍(扩展数据表10f),表明共享的压力分布反映了脆弱性和向衰老的过渡。瘦AT还含有大量(尽管明显较低)p21阳性细胞(图5b)。衰老的抑制反映了脂肪细胞生物能量学的增强,表明这些效应可能是机械耦合的(扩展数据图10h)。因此,我们确定人类WL具有以前未描述的强效senolytic作用。
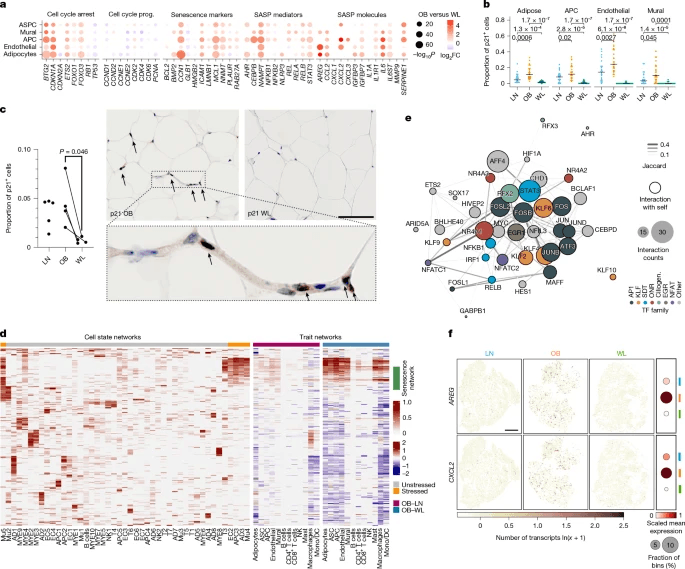
全组织基因调控网络分析揭示了应激衰老细胞中紧密保守的转录关系,在肥胖时增加,在WL时减少(图5d)。已鉴定的转录因子分为几类(图5e和扩展数据图10i)。这些分析揭示了退行性AT衰老周期的不同细胞内和细胞外介质,并支持AT衰老的逆转是WL代谢健康益处的关键决定因素。
研究中报告了接受治疗性WL的极度肥胖患者和健康瘦人AT的高分辨率单核和空间图谱。肥胖和WL的同时分析使我们能够了解核心组织重塑原理;捕获20多种随体重变化的细胞状态(包括桥接细胞本体的退化和适应性群体);并定义可能驱动组织损伤和随后恢复的分子途径、调节因子和细胞间信号。发现WL对脆弱细胞类型的衰老具有显著的缓解作用。研究得出结论,AT衰老的逆转可能是人类WL多器官抗炎和代谢益处的核心。
研究结果表明,WL对已知影响代谢健康和寿命的细胞过程有显著影响。更广泛地说,我们的研究结果强调了积极预防肥胖的必要性,并支持了持续的生活方式改变可能通过多种AT细胞类型的动态重塑而产生长期健康益处的可能性。人类AT生物学和病理生理学的丰富表现为机制和治疗探索提供了宝贵的资源
肥胖的危害

肥胖影响着全球超过10亿人。AT质量增加是肥胖的决定性特征,是2型糖尿病、心血管疾病、某些癌症和早期死亡的主要危险因素之一。通过减肥(WL)减少AT质量可显著改善肥胖引起的合并症,并可降低死亡率。对支持这些对比临床效果的生物学的协同和详细理解是改善治疗选择和健康结果的核心。
结 语
这项研究成果,如同一张高清地图,让我们看清了肥胖状态下脂肪微环境的衰老迷宫,也找到了减肥引领细胞走出困局的清晰路径。减肥这场看似外在的体型改变,实则是一场深入细胞层面的健康革命,它清扫脂肪组织中的衰老与炎症因子,为身体重启代谢平衡创造可能。
在全球肥胖率持续攀升的今天,这项研究不仅为肥胖患者带来了科学希望,更向所有人传递了一个重要理念:关注体重,更要关注体重背后的细胞健康。主动管理体重,就是为身体的细胞生态系统注入活力,从根源上抵御衰老与疾病,拥抱更健康的未来
参考文献
1:Selective remodelling of the adipose niche in obesity and weight loss
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

