
2026年2月12日,中山大学邝栋明,魏瑗和劳向明共同通讯在Nature Cell Biology 在线发表题为“THY1+ cancer stem cells drive metastasis through a pseudohypoxic state shaped by neutrophil-derived mitochondria”的研究论文。首次系统揭示中性粒细胞通过迁移体向THY1⁺肿瘤干细胞“递送”损伤线粒体,塑造其“伪缺氧”状态并驱动转移的全新机制。这一发现打破了传统肿瘤转移研究的认知边界,为理解肿瘤微环境与肿瘤干细胞的交互作用提供了全新视角,也为开发靶向肿瘤转移的新型疗法奠定了理论基础。

研究过程
关键肿瘤干细胞亚群的鉴定与验证
(一)临床样本与多组学分析
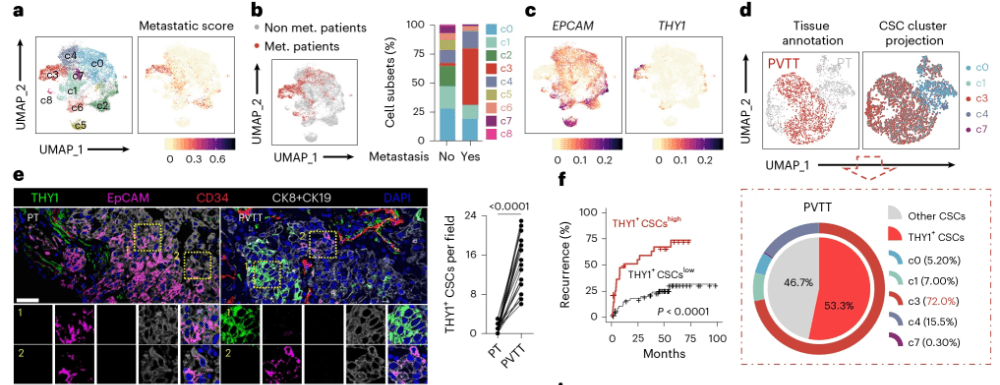
研究团队首先收集了94例肝癌患者样本,对共计125683个癌细胞进行单细胞RNA测序,从中鉴定出11589个肿瘤干细胞,并进一步划分为9个亚群。通过对比转移患者与非转移患者的细胞亚群分布,发现第3亚群(即THY1⁺ CSC)在转移样本中占比约50%,远高于非转移样本的不足2%,初步锁定其为具有强转移潜能的关键亚群。
同时,整合人类肿瘤单细胞转录组、空间转录组及泛癌分析数据,发现THY1⁺ CSC在乳腺癌、结肠癌、肺癌等多种实体瘤中高度保守存在,且显著富集于转移灶,与患者不良预后密切相关。
(二)动物模型验证转移潜能
为验证THY1⁺ CSC的转移能力,研究人员构建了多种荷瘤动物模型。将THY1⁺ CSC与EpCAM⁺ CSC分别原位接种于免疫健全小鼠,结果显示THY1⁺ CSC展现出强劲的肺转移潜能,显著缩短动物生存期;而遗传敲除或抗体阻断THY1则可有效抑制转移发生。
“伪缺氧”状态的发现与机制初探
(一)非缺氧依赖的代谢特征分析
通过基因集富集分析,研究人员发现THY1⁺ CSC显著富集缺氧相关转录程序,但空间转录组学分析显示,这些细胞常分布于血管丰富的氧合区域,并非处于传统的低氧环境。进一步的分子生物学实验证实,THY1⁺ CSC中的HIF1α蛋白在常氧条件下仍能稳定积累,逃避泛素-蛋白酶体降解,从而形成非缺氧依赖的“伪缺氧”状态。
(二)信号通路对CSC极化的调控
研究团队通过细胞培养实验发现,在IL-6–Myc信号轴的调控下,部分EpCAM⁺ CSC可向THY1⁺ CSC极化。当向细胞培养基中添加IL-6时,EpCAM⁺ CSC中THY1的表达水平显著升高;而抑制Myc的活性则可阻断这一极化过程,证实了IL-6–Myc信号轴在THY1⁺ CSC形成中的关键作用。
中性粒细胞与THY1⁺ CSC的交互作用机制
(一)细胞共培养与信号轴验证
将THY1⁺ CSC与肿瘤浸润中性粒细胞进行共培养,通过免疫荧光染色和免疫共沉淀实验,证实THY1⁺ CSC可通过THY1–Mac1信号轴与中性粒细胞发生特异性相互作用。当使用抗体阻断THY1或Mac1后,中性粒细胞的激活状态明显受到抑制。
(二)迁移体介导的线粒体释放观察
利用活细胞成像技术,研究人员实时观察到激活后的中性粒细胞以迁移体依赖方式排出富含活性氧的损伤线粒体。通过对迁移体进行分离纯化和成分分析,发现其中含有大量损伤线粒体,且这些线粒体的活性氧水平显著高于正常线粒体。
(三)巨胞饮作用与线粒体摄取验证
通过荧光标记线粒体实验,研究人员观察到THY1⁺ CSC可通过巨胞饮作用内化来自中性粒细胞的线粒体。当抑制巨胞饮相关蛋白的表达或使用巨胞饮抑制剂时,THY1⁺ CSC对线粒体的摄取能力显著下降,同时其“伪缺氧”状态和转移潜能也被削弱。
线粒体摄取对“伪缺氧”状态的调控机制
(一)活性氧对HIF1α稳定性的影响
将富含活性氧的损伤线粒体导入THY1⁺ CSC后,通过Western blot和免疫荧光染色发现,HIF1α蛋白的稳定性显著增强。进一步的机制研究表明,损伤线粒体释放的活性氧选择性抑制PHD2介导的HIF1α羟化修饰,从而阻止HIF1α被泛素-蛋白酶体降解。
(二)“伪缺氧”状态与转移能力的关联
通过基因敲降和过表达实验,研究人员证实HIF1α的稳定积累是THY1⁺ CSC获得转移潜能的关键。当敲降HIF1α的表达时,THY1⁺ CSC的侵袭和转移能力显著下降;而过表达HIF1α则可使EpCAM⁺ CSC获得类似THY1⁺ CSC的转移能力。
干预策略的功能验证
(一)信号通路阻断实验
在动物模型中,靶向IL-6–Myc、THY1–Mac1或Src–Akt/Erk信号通路进行干预,结果显示均可有效抑制伪缺氧驱动的CSC转移。例如,使用IL-6中和抗体或Myc抑制剂,可显著减少THY1⁺ CSC的形成,降低肿瘤转移率。
(二)线粒体释放与摄取抑制实验
通过抑制中性粒细胞的迁移体形成或阻断THY1⁺ CSC的巨胞饮作用,同样能显著削弱伪缺氧状态及其介导的转移过程。在小鼠实验中,使用迁移体抑制剂后,肿瘤肺转移灶的数量明显减少,动物生存期显著延长。
当遇到中性粒细胞时,THY1⁺ CSCs激活THY1–Mac1轴,触发Src–Akt/Erk通路、Rac1活化以及一种迁移体依赖的过程,该过程诱导中性粒细胞排出富含活性氧的受损线粒体。THY1信号进一步增强了巨胞饮作用,使得CSCs能够内化这些线粒体并进入假性缺氧状态,从而促进CSC转移。值得注意的是,靶向IL-6–Myc、THY1–Mac1或Src–Akt/Erk信号通路可有效抑制假性缺氧驱动的CSC转移。这些发现揭示了CSCs发生转移的先前未被探索的机制,为对抗肿瘤转移和改善癌症预后提供了潜在策略。
肿瘤
肿瘤转移是癌症患者死亡的首要原因,而肿瘤干细胞被认为是驱动转移的核心“种子”细胞。但并非所有肿瘤干细胞都具有同等的转移潜能,邝栋明团队通过整合人类肿瘤单细胞转录组数据、空间转录组学分析、泛癌队列分析及多种动物肿瘤模型,鉴定出一类在多种癌种中高度保守的肿瘤干细胞亚群——THY1⁺ CSC。
研究发现,THY1⁺ CSC显著富集于肿瘤转移灶,在肝癌门静脉癌栓中占比高达72%,且在乳腺癌、结肠癌、肺癌等多种实体瘤中均表现出显著的转移倾向,与患者不良预后密切相关。功能实验进一步证实,将THY1⁺ CSC与EpCAM⁺ CSC分别原位接种于免疫健全小鼠,前者展现出强劲的肺转移潜能,显著缩短动物生存期;而遗传敲除或抗体阻断THY1则可有效抑制转移发生。这一系列证据确立了THY1⁺ CSC作为肿瘤转移关键驱动者的核心地位。
中性粒细胞线粒体“递送”的精妙机制
研究团队进一步揭示了THY1⁺ CSC“伪缺氧”状态形成的关键机制——中性粒细胞通过迁移体介导的线粒体转移。这一跨细胞代谢重塑过程主要分为四个步骤:
信号激活
在IL-6–Myc信号轴驱动下,部分EpCAM⁺ CSC极化形成THY1⁺ CSC。当THY1⁺ CSC与肿瘤浸润的中性粒细胞接触时,通过THY1–Mac1信号轴激活中性粒细胞。
线粒体释放
激活后的中性粒细胞以迁移体依赖方式排出富含活性氧的损伤线粒体。迁移体作为一种新型细胞外囊泡,在此过程中扮演了“线粒体运输车”的角色。
线粒体摄取
THY1⁺ CSC通过THY1介导的巨胞饮作用内化这些来自中性粒细胞的线粒体。THY1过表达还会直接增强CSC的巨胞饮能力,进一步促进线粒体摄取。
代谢重塑
外源线粒体进入THY1⁺ CSC后,其携带的活性氧选择性抑制PHD2介导的HIF1α羟化修饰,稳定HIF1α蛋白水平,从而建立稳定的伪缺氧程序,显著增强THY1⁺ CSC的侵袭与转移能力。
结 语
邝栋明团队的这项研究在免疫学层面提出了三个重要认识:一是揭示了中性粒细胞通过线粒体转移直接调控肿瘤干细胞命运的新模式;二是建立了“免疫细胞来源线粒体—代谢重塑—肿瘤转移”这一跨细胞器调控轴;三是拓展了中性粒细胞在肿瘤免疫中的功能维度,从炎症调节延伸至代谢重编程调控。
未来,基于该研究成果,科研人员可进一步探索:不同癌种中THY1⁺ CSC的特异性调控机制;如何将这些潜在靶点转化为临床可应用的治疗药物;以及如何联合现有治疗手段实现对肿瘤转移的精准干预。相信随着研究的深入,这一发现将为攻克肿瘤转移这一医学难题带来更多突破。
参考文献
1:THY1+ cancer stem cells drive metastasis through a pseudohypoxic state shaped by neutrophil-derived mitochondria
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

