
在癌症治疗的漫长征程中,化疗耐药始终是横亘在医患面前的一座大山。尽管医学技术不断进步,仍有诸多患者在经历看似成功的治疗后,遭遇癌症复发的困境
长久以来,科学家们逐渐意识到肿瘤内部并非一片“净土”,尤其是在结直肠癌、口腔鳞癌等黏膜相关肿瘤中,细菌的存在已成为肿瘤微环境中不可忽视的组成部分。传统观点认为,肿瘤内的细菌多存在于细胞内,通过释放代谢产物、激活信号通路等方式促进肿瘤发展。然而,这项新研究却打破了这一固有认知,将目光聚焦于细胞外的肿瘤浸润细菌。
近期发表于《Cancer Cell》的一项题为“Tumor-infiltrating bacteria disrupt cancer epithelial cell interactions and induce cell-cycle arrest”的研究,为我们揭开了化疗耐药背后的全新机制——肿瘤浸润细菌竟能通过独特方式迫使癌细胞进入“休眠”状态,使其躲过化疗药物的杀伤,为癌症复发埋下隐患。

通过将PanCK+癌症细胞群的多重免疫组织化学(IHC)与靶向RNAscope相结合,以描述肿瘤组织中的细菌定位,我们鉴定了癌症上皮细胞,这些细胞位于人类OSCC和CRC样品中的细菌定殖微核内(图1A;图S1A-S1F)。苏木精和伊红(H&E)染色与病理学检查显示,瘤内细菌主要局限于肿瘤组织的坏死区域(图S1C和S1H)。高分辨率共聚焦显微镜使我们能够根据肿瘤内细菌状态准确定位癌症细胞核在肿瘤区域的空间分布(图1B)癌症上皮细胞的细胞分布和细菌负荷也与它们的增殖能力相关。与未感染肿瘤区域的癌症细胞相比,在细菌定殖的微针中,上皮癌症细胞表现出较低水平的Ki67表达,癌症细胞密度较低(图1D和1E)。
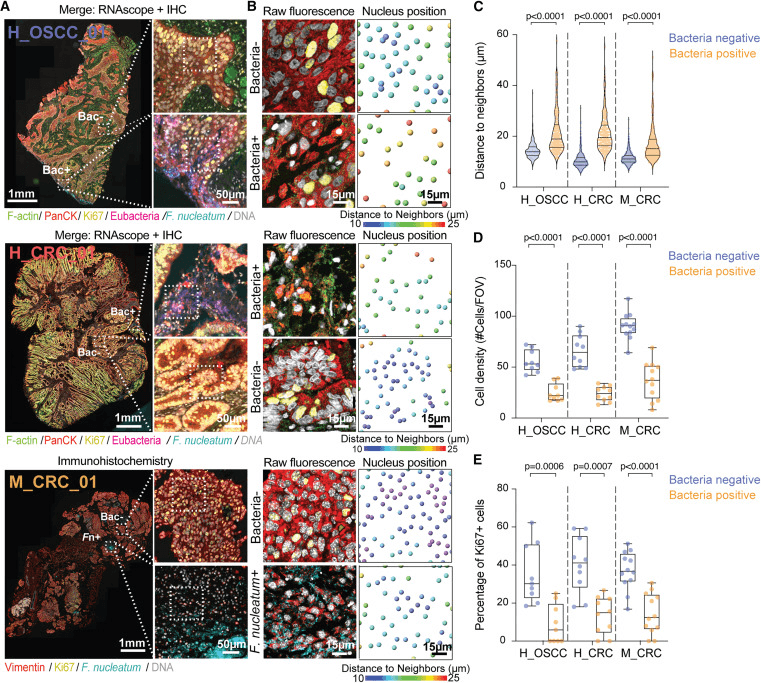
研究采用了带有皮下结肠癌癌症上皮肿瘤的同基因小鼠模型。小鼠静脉注射有核梭杆菌亚种的人CRC肿瘤分离物。动物(SB010、Fna C2)。注射后48-72小时,切除肿瘤并进行分析。RNAscope和带有SB010单克隆抗体的IHC均证实了F.nuclearum在不同肿瘤区域的定植,概括了人类OSCC和CRC样本的特征(图1A;图S1G)感染的肿瘤显示出比对照组更大的坏死区域,并含有富含细胞外细菌的微小颗粒(图S1I),细菌负荷存在显著差异(图S1J),只有少数宿主细胞位于定植区域(图S1K)。这些结果表明,肿瘤内细菌可以破坏上皮细胞与细胞的相互作用,调节癌症生物学中的基本信号通路,包括癌症细胞的增殖能力。
这些发现支持了CRC中富含细菌的微小突起与上皮组织破坏和增殖潜力降低有关的结论,并进一步强调了F.nuclearum是CRC患者中这些空间上不同的瘤内小生境的主要贡献者
在这些已鉴定的定植细菌中,我细菌载量为感染多样性(MOI),由每个宿主DAPI+细胞的16S或23S rRNA病灶数量定义。这些富含细菌的区域显示出细菌负荷的异质性分布,在一些肿瘤微通道区域,MOI范围为2至100以上(图S1J)。观察到细菌载量与细胞外细菌比例之间存在很强的正相关关系。MOI较高的肿瘤区域主要含有细胞外细菌(图2C)。在量化F.nuclearum病灶时出现了类似的模式,这些病灶主要出现在高负荷肿瘤区域的细胞外室中(图2D)
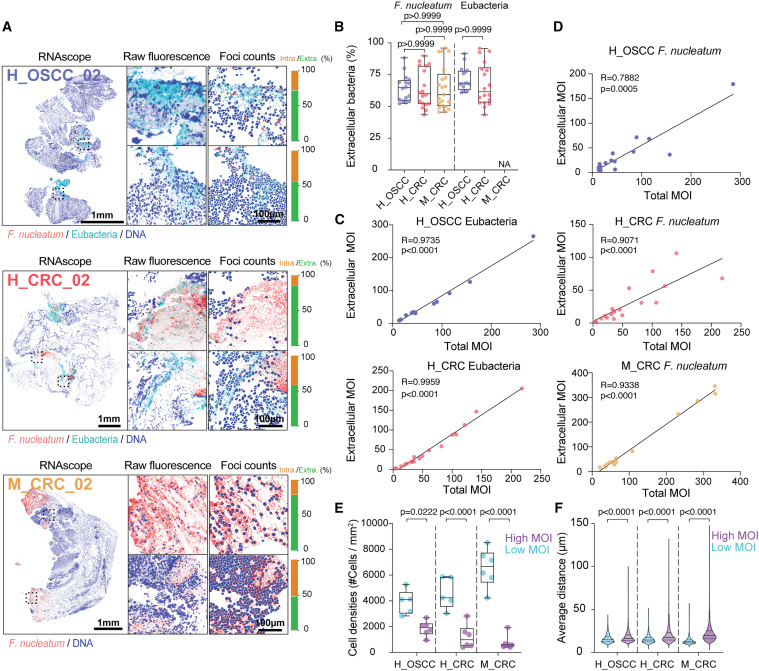
将两种微小型分为:相对较低的细菌载量(MOI<20;<25th百分位数)和相对较高的细菌载流量(MOI>80;>75th百分位)。高细菌载量微通道比低细菌载量区域含有更少的总DAPI+宿主细胞(图2E),并且显示出分散的分布,与五个最近的邻居有更大的平均距离(图2F)。这些模式在直肠原位模型中得到了进一步验证(图S3)。与皮下模型相似,F.nuclearum subsp。animalis定位于肿瘤组织内的微小切口(图S3A-S3C),并在感兴趣区域(ROI)显示出异质性感染率,MOI估计值超过100(图S3C)。观察到MOI与ROI的平均细胞间距离之间存在显著的正相关关系(图S3E),这进一步证实了我们的结论,即细菌载量增加与上皮细胞组织的破坏有关。这些空间特征概括了患者肿瘤中的结构,并证实了细胞外F.nuclearum在多个体内模型中重塑肿瘤微细结构的作用
总的来说,这些发现表明,肿瘤组织内的细菌定位是高度异质的,包括细胞内和细胞外的生态位,细菌感染率(MOI)范围很广。在较高的细菌负荷下,肿瘤内细菌主要定位于细胞外空间,即TME中细胞之间的物理存在,通过诱导较低的增殖率以不同的方式调节癌症生物学,如图1A所示。
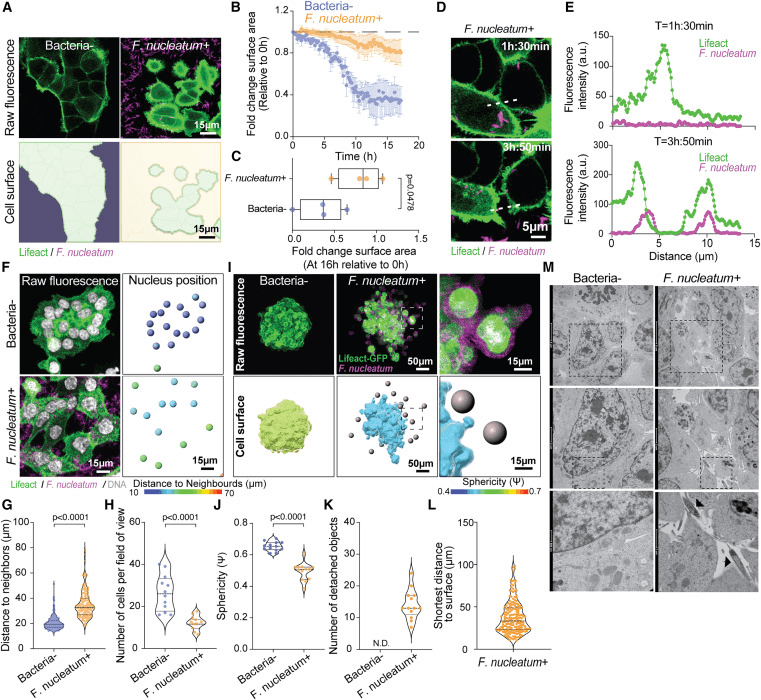
在无细菌对照中,上皮细胞作为一个整体在视野中扩大,表明上皮间接触完整(图3A和视频S1)。随着这些对照细胞的增殖,细胞外空间逐渐减少(图3B和3C)。相比之下,F.nuclearum暴露破坏了这些接触,分离了单个细胞并损害了单层扩张(图3A-3C和1K)。PI染色在整个成像过程中证实了上皮细胞的存活率(视频S1)。这些发现表明,在有核F.nucleanum存在的情况下,癌症细胞增殖受损,有核F.Nucleanum是我们在患者肿瘤组织中观察到的细菌高负荷区域的代表。
为了进一步研究肿瘤内细菌通过干扰细胞与细胞的相互作用对癌症细胞增殖能力的影响,研究人员使用FUCCI(荧光泛素细胞周期指示器)构建体来跟踪暴露于有核F.nucleum subsp。动物(SB010),MOI为0-100(图4A)。活细胞成像显示,F.nuclearum subsp。与对照相比,动物改变了在2D表面上培养的上皮癌症细胞的细胞周期行为(图4A)。图像分析表明,癌症上皮细胞与有核F.nucleum subsp。
实时细胞周期分析显示,在MOI 10和100时,G0-G1分数逐渐增加,10小时后G0-G1富集达到最大值,并在整个成像过程中持续存在(图4B-4E,视频S3)。G2-M组分呈相互下降趋势。未感染对照组(MOI 0)和MOI 1条件随时间波动,但没有净变化(图4E)。如前所述,细胞周期时间的随机变化对种群增长是必不可少的。这些结果表明,F.nuclearum亚种。动物暴露诱导G0-G1阻滞,从而增加非循环细胞的比例并抑制癌症细胞增殖
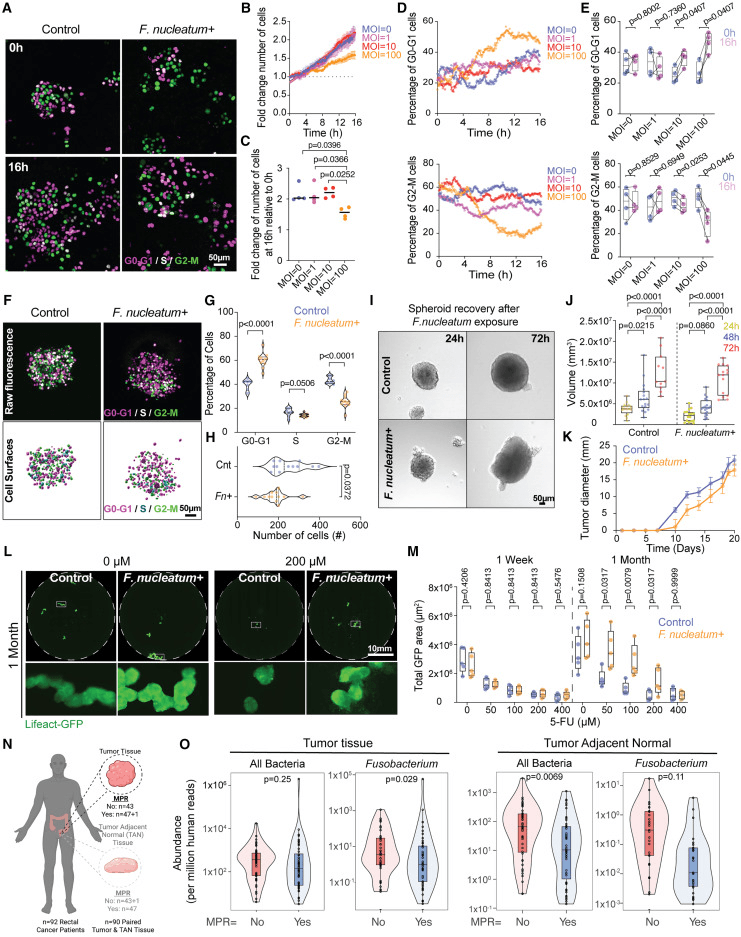
研究分析了92名直肠癌症患者在新辅助治疗后已知结果的预处理配对肿瘤和肿瘤邻近正常组织活检的全基因组测序数据51(图4N和4O),量化了这些组织中的总细菌负荷和梭杆菌负荷。与实现MPR的患者相比,未实现主要病理反应(MPR)的患者在其肿瘤邻近正常组织中的总细菌载量或拟杆菌载量明显较高,在其肿瘤组织内的总细菌负荷没有显著上升趋势(图4N;图S4B)。与应答者相比,无应答者肿瘤组织内的梭杆菌负荷显著升高(图4O)。
与未经处理的对照组相比,两种处理都增加了G0-G1细胞的比例,DMSO导致更大的G0-G1期阻滞(图5A和5B)和更大的细胞总数减少(图5C)。在去除化合物后,细胞重新建立了接触,在24小时内形成了小簇(图5D),其S和G2-M比例高于对照组(图S7A和S7B),表明细胞间相互作用影响了使细胞恢复细胞周期的信号通路。到72小时,预处理的细胞形成了与对照组大小相当的球体(图5D和5E),尽管恢复与初始G0-G1期阻滞相关:DMSO处理的细胞需要更长的时间才能达到大球体大小(图5E和5F)
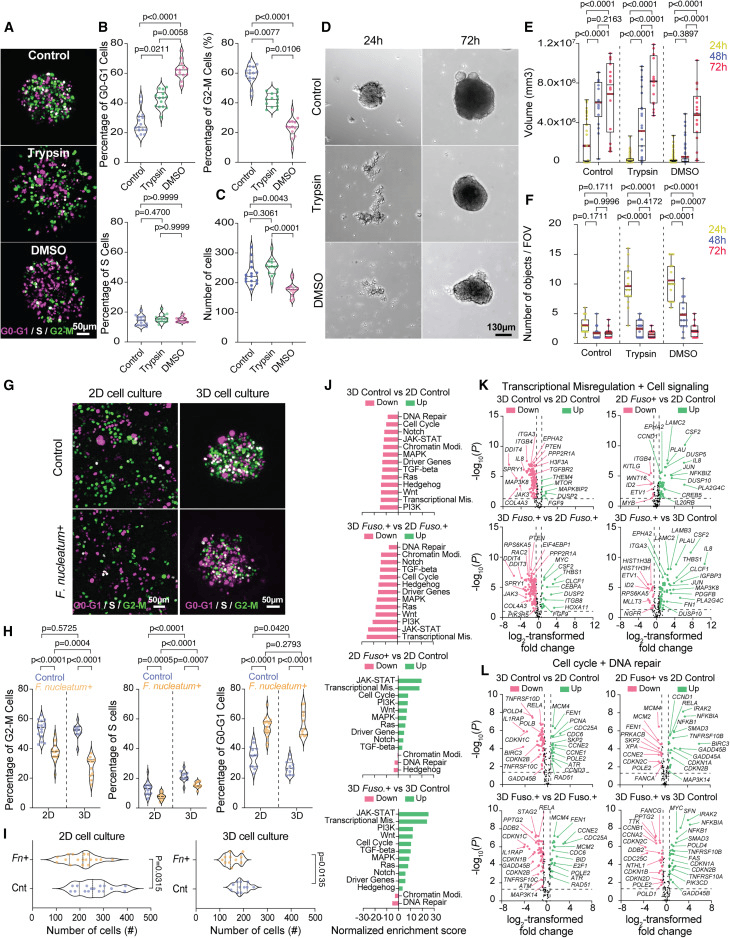
在肿瘤内,有核F.nucleum感染可引发炎症反应,重塑富含细菌的微核细胞的免疫景观,招募骨髓细胞,如巨噬细胞和中性粒细胞,抑制抗肿瘤T细胞活性并促进肿瘤生长。在系统中,有核F.感染后癌症进展和炎症相关基因的差异表达在3D培养物中比在2D培养物中更明显,这表明2D表面配体可能抑制细菌在癌症上皮细胞中的促肿瘤和促炎作用。
上皮癌症细胞与患者肿瘤来源的坏死F.necophorum菌株共同培养。随后的成像证实,F.necrophorum细胞仍主要位于细胞外,与F.nuclearum相比,在2D培养中的侵袭能力明显较低(图6A-6C)。
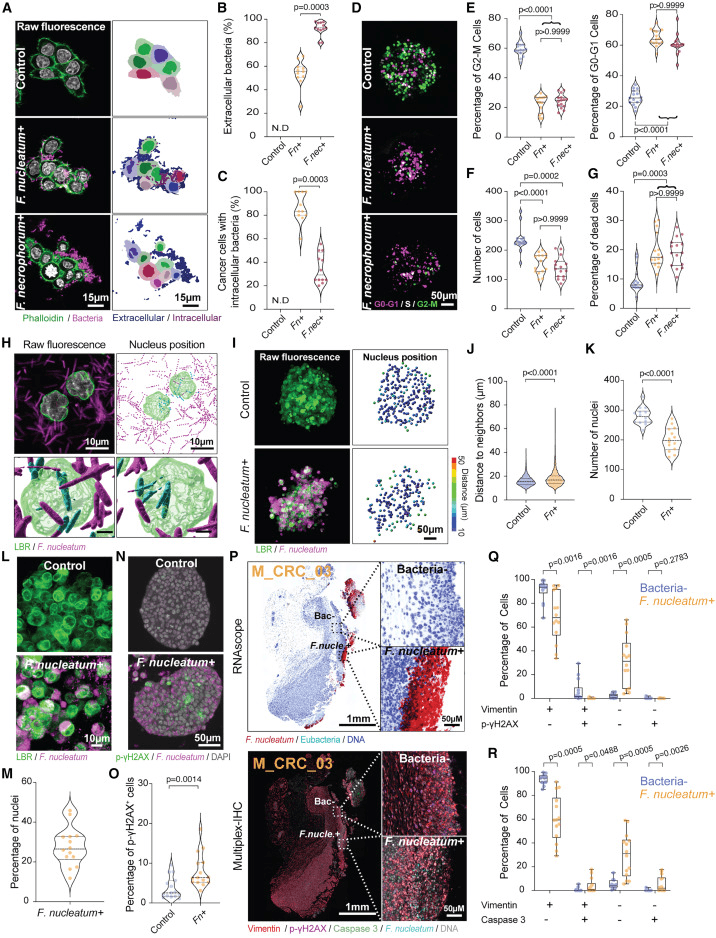
使用图1F中描述的同基因小鼠模型,我们发现与同一肿瘤的其他区域相比,有核F.nucleanum定位于Vimentin+/p-γH2AX+癌症细胞密度较低的微核。使用裂解的胱天蛋白酶3染色的进一步分析显示,F.成核定殖微核内的大多数癌症细胞是活的(Vimentin+/Caspase3-)(图6R)与无细菌区域相比,在这些小生境中存在少量但显著比例的波形蛋白+/胱天蛋白酶3+细胞,这表明肿瘤内细菌感染可能触发上皮癌症细胞亚群的凋亡。这一观察结果与我们的体外数据(图6K)和之前的一份报告一致。
使用CosMx-SMI空间单细胞转录组学,我们描述了人类CRC肿瘤中融合杆菌定殖微核内的上皮癌症细胞。靶向RNAscope证实患者肿瘤组织内存在细菌定植的微小突起(图7A)。对CosMx SMI的连续切片进行PanCK(上皮)、CD45(免疫)和ATP1B3(膜)染色,以进行单细胞分割(图7A)
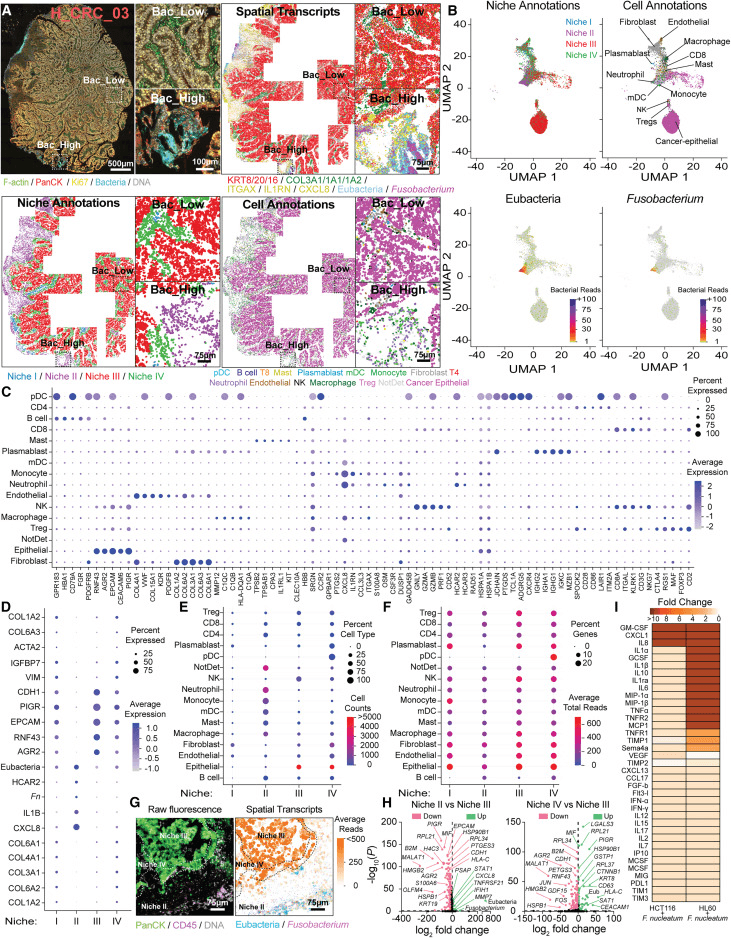
研究人员用HCT-116上皮细胞或HL-60中性粒细胞进行了体外3D共培养实验,其中有和没有肿瘤衍生的F.nuclearum亚种。动物菌株(SB010)。共培养24小时后,融合菌-暴露的癌症上皮细胞在上清液中产生GM-CSF、CXCL1和CXCL8,其水平与融合菌-释放的中性粒细胞相当(图7I)。这些发现表明,在患者肿瘤细菌感染壁龛内和周围的上皮细胞中观察到的炎症基因特征(图7H)积极促进了针对肿瘤内细菌的炎症反应(图7I)。
这项研究通过整合正交方法,包括人类肿瘤的空间成像和单细胞空间转录组学、活细胞成像、与肿瘤衍生细菌分离株的3D共培养以及小鼠研究确定了一种以前未被识别的机制,肿瘤浸润细菌通过该机制积极调节TME内的癌症上皮细胞行为。在富含细菌的微生态位中,癌细胞呈现出明显的转录静止表型,其人类转录本总数显著减少。更危险的是,这些癌细胞下调了抗原提呈基因(如HLA分子)以及CAR-T治疗靶点(如EPCAM、EPHA2等)的表达,这可能极大地削弱了T细胞的识别能力,帮助癌细胞实现免疫逃逸。
细菌使癌细胞休眠的机制
细菌让癌细胞“装睡”的核心机制,是胞外细菌通过物理破坏癌细胞间的连接,迫使癌细胞进入细胞周期停滞的休眠状态,从而逃避化疗药物的杀伤
01物理挤压与空间重塑
细菌并非侵入细胞内部作祟,而是在细胞外“安营扎寨”。在高细菌负荷区域,癌细胞密度显著降低,细胞间距增大。实验证明,若人为破坏上皮细胞间的接触(模拟细菌作用),癌细胞也会进入同样的休眠状态;反之,若恢复细胞接触,癌细胞可重新苏醒并增殖。
02信号通路的“关闭”
细菌的干扰导致癌细胞内关键基因表达下调,特别是涉及细胞周期调控、转录和抗原呈递的基因。这使得癌细胞暂时“关闭”了生长开关,进入一种类似干细胞的可塑性状态,既能抵抗治疗,又能在环境适宜时快速“觉醒”。
03微环境的协同保护
细菌诱导的休眠不仅仅是细胞个体的行为,还重塑了局部微环境。休眠细胞分泌的因子可抑制免疫细胞活性,甚至招募巨噬细胞形成“保护罩”,进一步巩固其休眠状态,使其成为肿瘤治疗的“漏网之鱼”。
结 语
《Cancer Cell》上的这项研究如同照亮黑暗的一束光,让我们对癌症化疗耐药机制有了全新的认识。肿瘤浸润细菌通过物理挤压破坏癌细胞间连接,诱导细胞周期停滞,使癌细胞进入休眠状态,从而逃避化疗药物的杀伤。这一发现不仅为癌症治疗带来了新的靶点和思路,也提醒我们在癌症治疗中不能忽视肿瘤微环境中微生物的作用。
在未来的研究中,我们需要进一步深入探究细菌与癌细胞相互作用的具体分子机制,开发出更加精准、有效的干预手段。同时,开展大规模的临床研究,验证以肿瘤内细菌为靶点的治疗策略的安全性和有效性。相信随着研究的不断深入,我们终将攻克化疗耐药这一难题,为癌症患者带来更多的希望和福音。
参考文献
1:Tumor-infiltrating bacteria disrupt cancer epithelial cell interactions and induce cell-cycle arrest: Cancer Cell
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

