
2026年2月4日,加州大学圣地亚哥分校Wang Wei等团队合作在Nature 在线发表题为“Atlas-guided discovery of transcription factors for T cell programming”的研究论文。为T细胞编程的研究带来了革命性突破。该研究通过构建整合多维度数据的综合图谱,系统揭示了驱动不同CD8+ T细胞状态的转录因子,为免疫治疗、自身免疫病干预等领域开辟了全新的精准化路径。

研究人员开发了一个多组学图谱,整合了来自9个CD8+T细胞的转录组学和染色质可及性数据 了解每种细胞状态中TFs的“全局”影响,并识别“选择性”或“共享”TFs。基于图谱的平台可以绘制TF群落及其靶基因(“受调节者”),指导特定状态的分化。
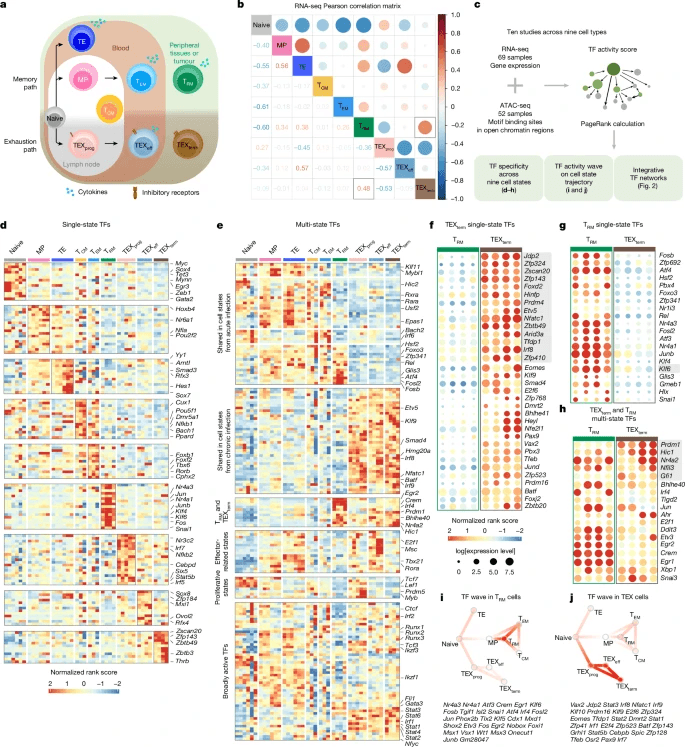
首先,研究人员使用来自121个CD8+T细胞的测序(ATAC-seq)和RNA测序(RNA-seq)数据集分析了转座酶可及染色质的测定 跨越九个不同状态的细胞样本,使用先前发表的和新生成的数据集,这些数据集来自特征明确的急性和慢性淋巴细胞性脉络丛脑膜炎病毒(LCMV)感染(扩展数据图1e和补充表1)。在急性LCMV-Armstrong感染中,CD8+T 细胞分化为记忆前体(MP)、末端效应器(TE)、效应器记忆(TEM)、中央记忆(TCM)和TRM状态。慢性LCMV中的克隆感染后,它们采用异质性耗竭细胞状态,包括耗竭祖细胞(TEXprog)、效应样耗竭(TEXeff)和TEXterm状态(图1a)。
尽管TEXterm和TRM细胞之间存在很强的转录重叠,但我们的太极管道预测TFs在这两种细胞状态中都是选择性活性的。这可能有助于开发更好的免疫疗法,在这种疗法中,人们可以设计T 细胞远离疲劳,朝向功能更强大的效应细胞状态,而不会对组织和肿瘤中的TRM细胞形成产生负面影响。根据统计标准(扩展数据图2a),我们分别确定了20个和34个TFs为TRM和TEXterm细胞的单态TFs,以及30个在两者中都活跃的多态TFs(图1f-h,扩展数据图2a(蓝色框)和补充表3)。
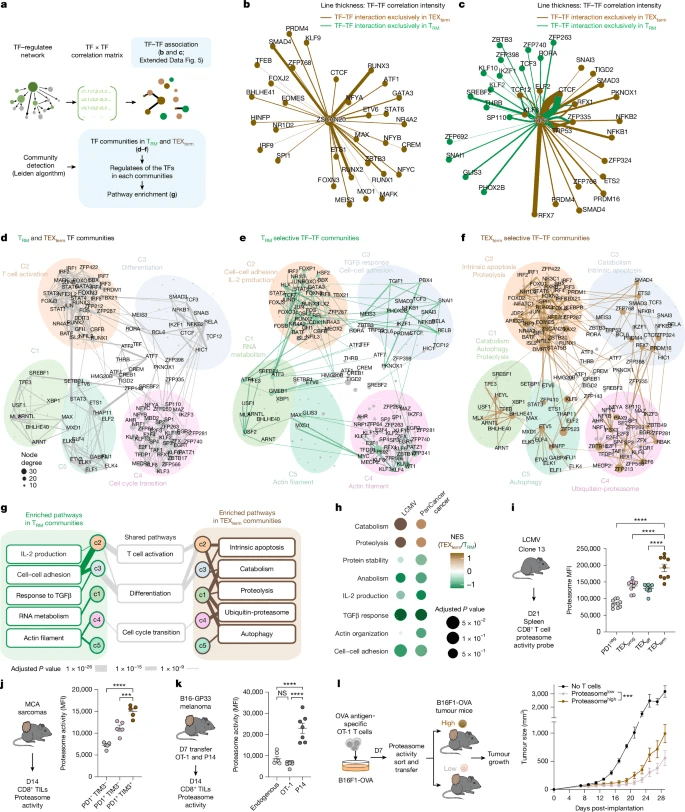
接下来,将TF-TF关联网络分为TRM和TEXterm细胞中不同的“TF邻居群落”(补充表5),每个群落都与特定的生物过程有关(图2d-f)。尽管多状态TF塑造了整个社区的拓扑结构,但单状态TF驱动了每个社区内TRM或TEXterm细胞特有的独特交互模式。通路分析揭示了每个州不同的程序——例如,TRM社区-3与细胞粘附和TGFβ反应有关(图2e,g,h),而TEXterm社区-3与凋亡有关(图2f-h)。TRM细胞中的Community-1控制着RNA代谢(图2e,g,h),而在TEXterm细胞中,它与分解代谢、蛋白水解和自噬有关(图2f-h)。
重点研究了蛋白酶体途径,这是TEXterm细胞的一个突出但以前未被认识的特征(图2g,h)。蛋白酶体基因特征在TEXterm样CD8+T中富集 来自非小细胞肺癌(NSCLC)患者44和小鼠MCA-205 TIL的细胞(扩展数据图5a,b)。与旁观者OT-1细胞(图2k)相比,蛋白酶体活性(通过验证的荧光探针45测量)在慢性LCMV的TEXterm细胞(图2i)和肿瘤特异性TIL(图2j,k)中最高。
多态TF基因包括两个阳性对照(Nr4a2、Prdm1)和未验证的多态TF基因(Nfil3、Hic1、Gfi1、Ikzf3、Stat3)。为了确保全面筛查,每个靶点有四个gRNA在两个双gRNA逆转录病毒载体中表达(扩展数据图6a),以及两个带有加扰gRNA的对照载体(gSamble)。这创建了一个包含40个双gRNA载体的文库,其中包含76个TF-gRNAs和4个gScramble对照(补充表6)。
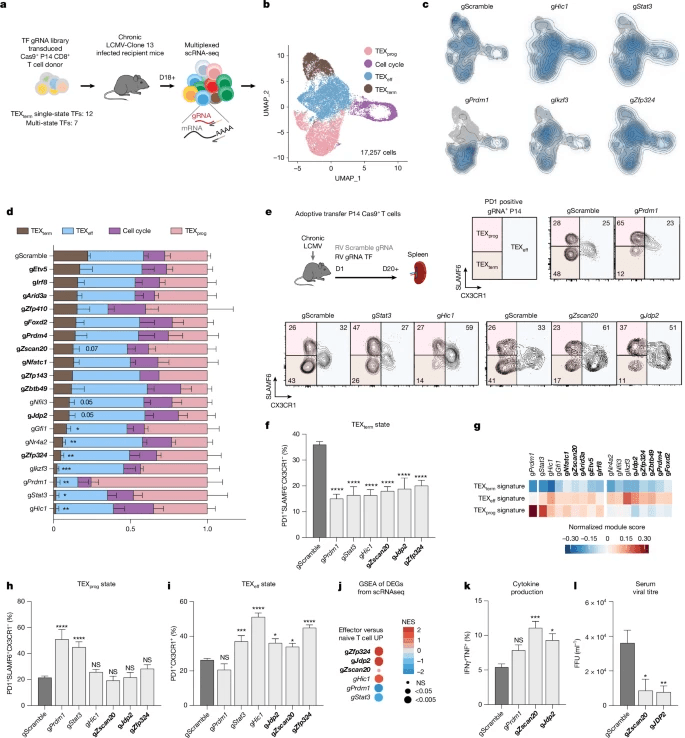
Cas9+P14 CD8+T 用该文库转导细胞,并将其转移到感染LCMV-Clone-13的小鼠体内,这是一种慢性感染和CD8+T的模型 细胞耗竭(受体小鼠也表达Cas9以防止供体细胞排斥)。转移后18天或更长时间进行基于液滴的测序,以评估每个脾脏来源的供体Cas9+P14 CD8+T细胞的sgRNA和转录组(图3a),分析17257个具有独特gRNA表达的细胞。
通过分析gRNA+细胞在耗竭状态下的分布来评估单个TF耗竭的影响(图3c,d)。19个驱动TEXterm的TF基因中的大多数被CRISPR敲除(KO),导致TEXterms细胞频率降低。值得注意的是,Hic1、Stat3、Prdm1和Ikzf3(编码AIOLOS)等多态TF基因的KOs导致TEXterm分化显著降低了约90%。新的TEXterm单态TF基因(包括Zfp324、Zscan20和Jdp2)的耗竭分别显著降低了TEXtterm分化78%、54%和43%(图3d,粗体)
研究使用流式细胞术和scRNA-seq分析TF-KO细胞 13 感染(图3e-i和扩展数据图6)。测试了六种TF-KO,包括已知的对照(Prdm1)和五种新鉴定的TF基因(Zscan20、Jdp2、Zfp324、Stat3、Hic1),这些基因在Perturb-seq中损害了TEXterm状态分化。破坏这些TF会使TEXterm细胞(PD1+CX3CR1−SLAMF6−)的频率降低约50%(图3e,f),并降低CD101、CD39和CD38等抑制性受体的表达(扩展数据图6d,e)。所有19个TEXterm TF基因KOs均表现出TEXtterm特征基因46的显著减少,包括Cd7、Cxcr6、Nr4a2和Entpd1(图3g)。
Zscan20和Jdp2的缺失显著增强了效应细胞因子的产生(例如,干扰素γ(IFNγ)和肿瘤坏死因子(TNF)),并降低了受体小鼠的病毒载量(图3k,l)。
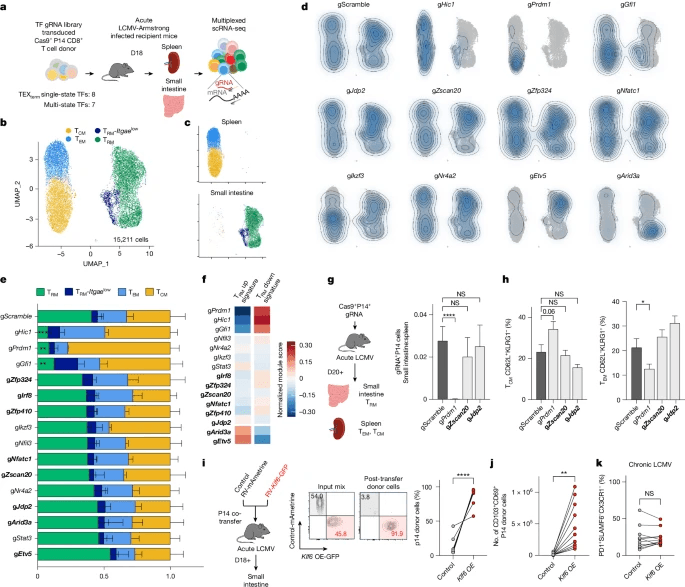
这些TFs在慢性LCMV感染中使TEXtterm状态发育受损25%以上(图3d),评估它们对记忆CD8+T的影响 在细胞发育过程中,分离出转导Cas9+P14 CD8+T的逆转录病毒 小鼠脾脏和小肠细胞18 急性LCMV-Armstrong感染后几天。然后,使用scRNA-seq分析了15211个细胞,以确定这些扰动如何影响肠道TRM细胞以及循环脾脏TCM和TEM细胞的形成(图4a)。
总的来说,这个多组学管道预测了TEXterm单态TFs和多态TFs,前者在不影响TRM细胞形成的情况下驱动TEXterms分化,后者影响两种细胞状态。这些结果证明了研究的方法在精确定位单态和多态TF方面的准确性和预测能力。
为了评估在人类T细胞中的小鼠发现的相关性细胞,特别是用于免疫治疗的应用,使用公开可用的单细胞多组学和来自人类肿瘤浸润CD8+T细胞的scRNA-seq数据集进行了跨物种验证 单元格(图5e,扩展数据图9a和补充表1)。利用太极TF分析平台,将小鼠TEXterm相关和TRM相关的TF基因映射到精心策划的人类全癌细胞CD8+T上 细胞图谱包括六种肿瘤类型(胶质母细胞瘤(GBM)、头颈部鳞状细胞癌(HNSCC)、基底细胞癌(BCC)、肝细胞癌(HCC)、肾细胞癌(RCC)和透明细胞肾细胞癌)。
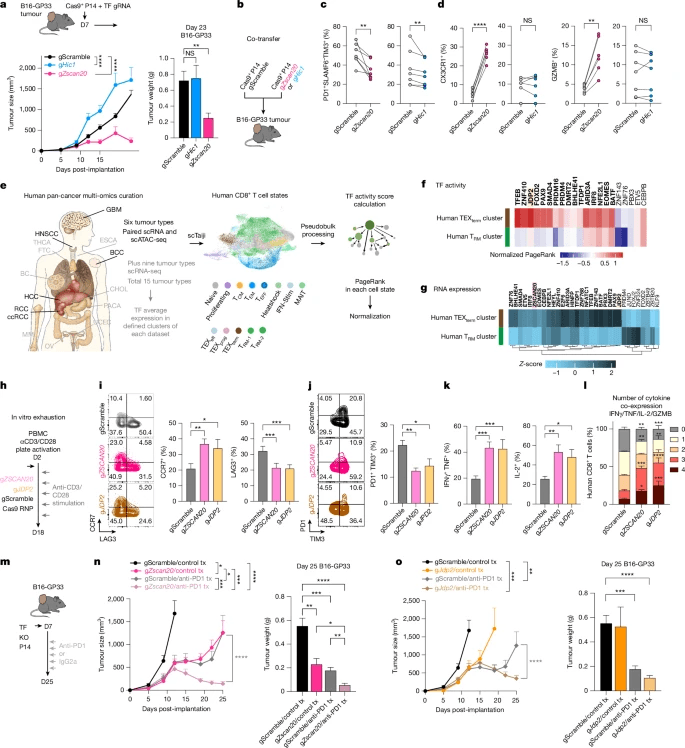
在34个小鼠TEXterm单态TF基因中,19个在人类TEXterms细胞中显示出保守的活性模式。同样,TRM特异性TF基因(例如NR4A1、KLF6和FOSB)在人类TRM簇中显示出丰富的活性(扩展数据图9c)。此外,在TEXterm和TRM状态下都活跃的30个小鼠TF基因中,有22个在人类数据集中显示出相似的活性特征(扩展数据图9d)。
在18岁以上重复CD3/CD28刺激后 模拟慢性激活的天数(图5h),ZSCAN20-或JDP2缺陷CD8+T 细胞表现出CCR7(幼稚/干细胞记忆/TCM标志物)表达增加和抑制性受体水平降低,包括LAG3、PD1和TIM3(图5i,j)。这些KO细胞还产生了更高水平的效应细胞因子(图5k,l),表明ZSCAN20和JDP2有助于人类CD8+T细胞的耗竭相关特征细胞。
这项研究的关键成果之一是鉴定了新的TFs,包括ZSCAN20和JDP2,作为TEXterm单态TFs,KLF6作为TRM单态TF,以及新发现的HIC1和GFI1等多态TFs的作用。扰动TEXterm单态TF不仅可以防止T 细胞耗竭,但也保留了这些细胞分化为效应器和记忆状态的能力。这导致了肿瘤控制的显著改善。通过将耗竭型 TEX 选择性机制与保护性 TRM 细胞程序相分离,该研究能够实现对 T 细胞状态的更精确调控,从而加速更有效细胞免疫疗法的合理设计。
T细胞编程:免疫调控的核心战场
在免疫系统中,T 细胞具有多种分化状态,尤其是幼稚T 细胞在各种免疫环境中分化为具有不同功能和运输模式的不同状态,如肿瘤和病毒感染。
CD8+ T细胞作为免疫系统中的“精锐杀手”,在抗病毒感染、抗肿瘤免疫中发挥着不可替代的作用。它并非单一功能的细胞群体,而是能分化为效应T细胞、记忆T细胞、耗竭T细胞等多种功能状态,不同状态的T细胞在免疫反应的启动、维持与消退中各司其职。例如,效应T细胞能快速识别并清除被病原体感染的细胞或肿瘤细胞;记忆T细胞则能在体内长期存活,当相同病原体再次入侵时迅速激活,提供持久的免疫保护;而耗竭T细胞则常见于慢性感染或肿瘤微环境中,其功能受损,无法有效发挥免疫杀伤作用。
长期以来,科学家们致力于解析调控T细胞状态转换的分子机制,期望通过人为干预T细胞的编程过程,增强其免疫功能,或纠正其异常分化。然而,T细胞的状态调控是一个复杂的网络,涉及众多转录因子、表观遗传修饰及信号通路的协同作用,传统研究手段难以系统地厘清其中的关键调控节点。
结 语
加州大学圣地亚哥分校Wang Wei团队的这项研究,通过构建综合的转录与表观遗传图谱,系统揭示了驱动CD8+ T细胞不同状态的关键转录因子,为T细胞编程的研究带来了范式性的转变。这一成果不仅深化了我们对T细胞免疫调控机制的理解,更为免疫治疗、疫苗研发等领域提供了重要的理论基础与潜在的治疗靶点。在未来的研究与临床应用中,这一成果有望推动精准免疫治疗的发展,为更多患者带来福音,开启免疫学与医学领域的全新篇章
参考文献
1:https://www.nature.com/articles/s41586-025-09989-7
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

