
在生命活动的精密调控网络中,细胞增殖是生物体生长、发育和修复的核心过程,而这一过程的稳定运行离不开各类“分子卫士”的保驾护航。核酸酶-解旋酶DNA2就是其中一员,它作为多功能基因组保护因子,从酵母到人类等多种生物的细胞增殖都依赖于它的正常功能。
英国萨塞克斯大学Ulrich Rass团队在Nature 在线发表题为“DNA2 enables growth by restricting recombination-restarted replication”的研究论文,该研究利用酵母和人类细胞证明,DNA2 抑制同源重组重启复制以及停滞的 DNA 复制叉处的检查点激活。在人类细胞中,当 DNA2 被降解时,这种控制机制的丧失会导致重组依赖性的 DNA 合成以及在细胞周期的 G2 期积累与 RPA 结合的单链 DNA。为我们揭开了DNA2调控细胞增殖、维护基因组稳定的全新机制,也为相关疾病的研究提供了重要的理论依据

cdc27-D1恢复了dna2-2细胞减少的细胞活力(扩展数据图3d).Dna2和Pfh1之间的相互作用也得到了类似的结果,Pfh1是有效D-环进展所需的解旋酶36。因此,编码核排除型38 pfh1的pfh1-mt抑制了RTS1的过度重组、检查点激活和dna2-2细胞的存活率低(扩展数据图3a至d)。
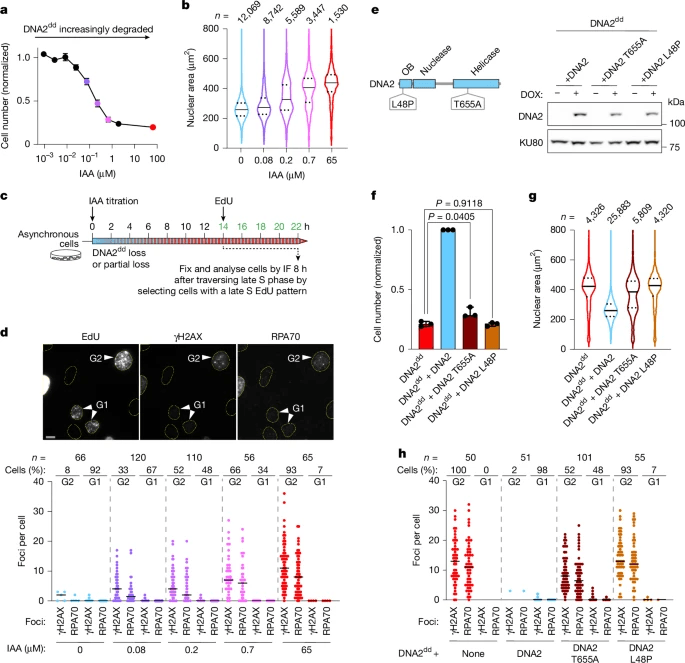
研究人员将迷你生长素诱导的degron(mAID)和小分子辅助关闭(SMASh)标签41的编码序列引入人上皮RPE-1细胞,以替换DNA2每个基因组拷贝的终止密码子(扩展数据图 4a).细胞还被修饰为多西环素诱导的水稻TIR1(OsTIR1)的表达,以通过mAID42实现受控的靶蛋白降解。通过添加多西环素与生长素吲哚-3-乙酸(IAA)和/或阿修那普利(Asv)的组合,可以激活SMASh标签介导的蛋白质降解,从而降解产生的双德隆标记的DNA2蛋白(DNA2dd)。在RPE-1 OsTIR1 DNA2dd细胞中加入强力霉素/IAA/Asv(DIA)药物混合物后,在4小时内不再检测到DNA2dd h(图 1a).
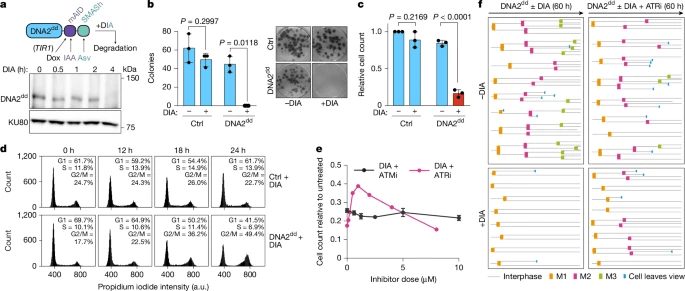
在克隆细胞存活试验中,向RPE-1 OsTIR1 DNA2dd细胞中添加DIA可消除集落形成(图1b) 并阻断细胞增殖(图。 1c).为了验证观察到的生长缺陷与DNA2的缺失有因果关系,用野生型DNA2互补DNA(cDNA)补充RPE-1 OsTIR1 DNA2dd细胞,在DNA2dd降解后恢复细胞增殖和集落形成(扩展数据图。 4b,c).
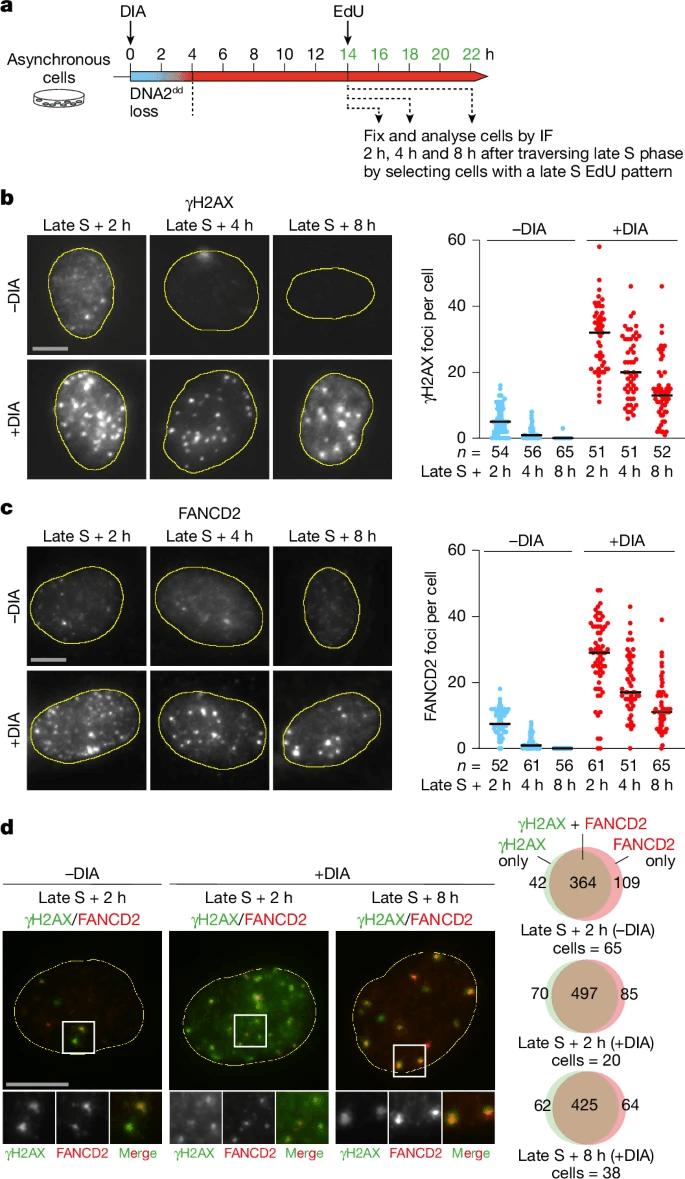
观察到具有降解DNA2dd的新生子细胞甚至没有经历一次随后的有丝分裂;这种对细胞分裂的恒定阻断可以通过添加ATRi来抑制,使细胞能够通过有丝分裂进行并形成活的子细胞(图。 1f和扩展数据图。 4d,e).
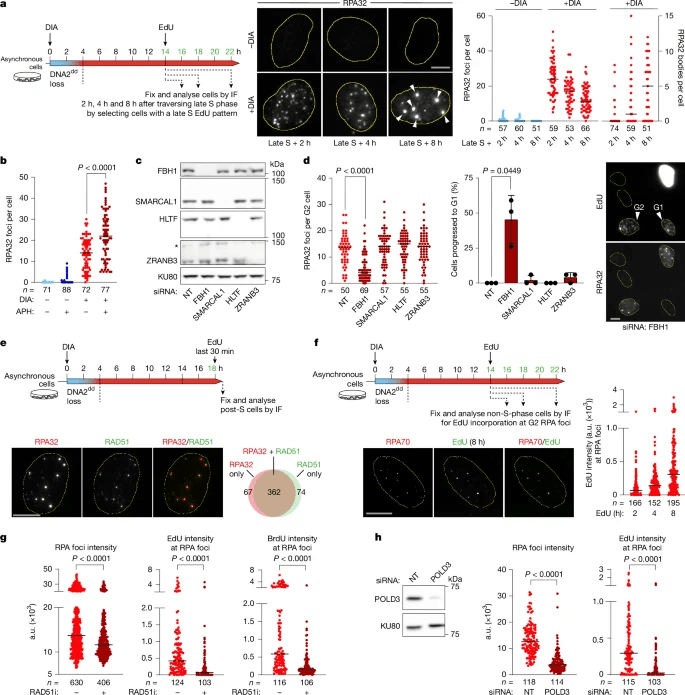
FBH1的耗竭,但SNF2易位酶的耗竭,显著减少了DIA处理的RPE-1 OsTIR1 DNA2dd细胞中的RPA灶(图。 3c,d).其中FBH1耗竭明显完全抑制了持续RPA-ssDNA积累的DNA2剥夺细胞亚群能够进行有丝分裂(图。 3d).HoRReR还取决于重组因子RAD51的链交换活性。发现RAD51标记了DNA2缺失细胞中的大多数RPA病灶(图。 3e). 短干扰RNA(siRNA)介导的Polδ亚基POLD3耗竭强烈抑制了DNA2剥夺细胞RPA病灶处的DNA合成(图。 3h).这些结果与同源重组依赖性DNA合成一致,该合成发生在迁移的D-环中,其中缠绕出来的新生ssDNA链在其尾部被RPA结合。
为了监测DIA处理后RPE-1 OsTIR1 DNA2dd细胞中的ATR活化,我们仔细检查了ATR激酶活性的靶标CHK1。CHK1磷酸化非常突出添加DIA后h,CHK1蛋白逐渐丢失(图。 4a) ,先前在G2细胞周期观察到的表型在外源DNA损伤后退出。
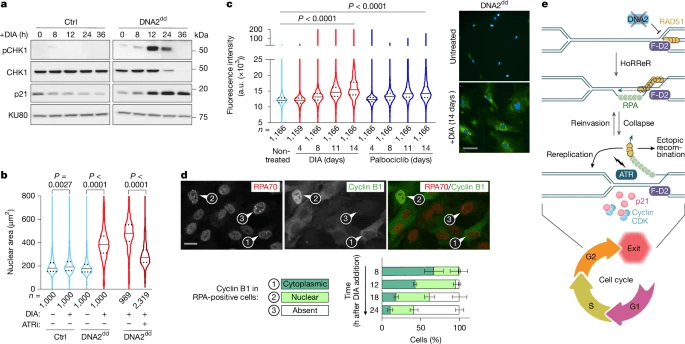
研究人员观察到G2中RPA病灶的形成首先与细胞周期蛋白B2从细胞质向细胞核的易位相关,然后与大多数RPA阳性细胞中细胞周期蛋白B124的丢失相关 添加DIA后h(图。 4d).只有一小部分细胞(18岁后约5%)显示S4和S8上RPA32的DNA双链断裂特异性磷酸化(pRPA),这总是与核或缺失的细胞周期蛋白B1相吻合(扩展数据图。 9e)
研究得出结论,需要依赖DNA2的叉加工来抑制停滞的复制中间体、HoRReR和细胞周期退出的积累,这为为什么DNA2对细胞增殖至关重要提供了新的解释(图。 4e).
报告表明,在培养的患者成纤维细胞中观察到与DNA2相关的小头畸形原始侏儒症、Seckel综合征和Rothmund-Thomson相关综合征中野生型DNA2的低浓度,以及衰老细胞。为了模拟DNA2浓度降低的影响,我们用强力霉素处理RPE-1 OsTIR1 DNA2dd细胞,并滴定IAA以逐渐诱导mAID降解标签(扩展数据图。 11a).在低IAA浓度下,细胞增殖基本不受影响,细胞核没有增大高IAA浓度阻碍了增殖,细胞显示细胞核增大,表明细胞周期退出,正如DNA2完全丧失所预期的那样。中等IAA浓度允许RPE-1 OsTIR1 DNA2dd细胞增殖,尽管增殖速率降低(图。 5a).在这些中等IAA浓度下,细胞分离成两个不同的群体,核大小正常或增大(图。 5b).因此,单个细胞退出细胞周期的倾向随着DNA2浓度的降低而增加。
研究表明,重组依赖性DNA合成的遗传扰动可以挽救Dna2突变细胞中过度的HoRReR、检查点激活和细胞周期阻滞。因此,Dna2功能障碍通过不受限制的HoRReR在远亲酵母物种中持续的G2/M检查点阻滞导致不可见。
实验性DNA2下调和Seckel综合征患者衍生的DNA2-T655A亚型的表达表明,存在一个临界水平的DNA2活性,在该水平下,细胞可以继续增殖而不会出现明显的DNA损伤,也可以进入HoRReR诱导的衰老。
01 DNA2是什么
DNA2是一种兼具核酸酶和解旋酶活性的多功能蛋白,长期以来,科学家们就知道它对细胞增殖至关重要,但在缺乏DNA2的情况下阻止细胞增殖的具体机制,以及DNA2相关疾病的分子病因却一直迷雾重重。此前的研究认为,DNA2在滞后链复制过程中对冈崎片段的加工发挥着关键作用,它能够切割由单链DNA结合蛋白RPA结合的5'块状结构,而这些结构难以被冈崎片段加工核酸酶FEN1作用。如果没有DNA2,这类块状结构可能会累积,进而激活DNA损伤检查点,这也解释了酵母中因失去DNA2而发生的致命G2/M检查点停滞现象。不过,关于DNA2缺陷酵母细胞中是否存在有毒的冈崎片段连接块状结构仍不明确,且人类DNA2在冈崎片段加工过程中的作用也缺乏直接证据。

02 DNA2限制重组重启复制的核心机制
Ulrich Rass团队的研究通过酵母和人类细胞实验,终于破解了这一难题,揭示了DNA2在细胞增殖和基因组稳定维护中的全新作用机制。
研究发现,DNA2能够抑制同源重组重启复制以及停滞的DNA复制叉处的检查点激活。在正常情况下,当DNA复制过程中遇到阻碍,复制叉停滞时,细胞会启动一些应急机制来试图重启复制,其中同源重组重启复制就是一种途径。但这种途径如果不受控制,可能会导致基因组的不稳定性,进而影响细胞的正常增殖。DNA2就像一个“调控开关”,严格限制着这种重组重启复制的发生,确保DNA复制过程的有序进行。
当人类细胞中的DNA2被降解时,这种调控机制就会丧失,细胞内会出现重组依赖性的DNA合成,并且在细胞周期的G2期积累大量与RPA结合的单链DNA。这些异常变化会触发DNA损伤检查点,最终导致在有丝分裂前由ATR-p21依赖性的细胞周期退出。这一过程解释了为何DNA2对细胞增殖至关重要。一旦DNA2功能缺失,细胞就无法正常完成细胞周期,增殖过程被阻断。
此外,研究还发现,DNA2的功能异常与细胞衰老密切相关。当表达来自Seckel综合征患者的DNA2低效突变体,或者DNA2部分降解时,细胞会随机进入衰老状态,增殖能力受到抑制。这一发现为解释与DNA2相关的原始矮小症疾病中的整体生长障碍提供了关键的概念框架,让我们对这类疾病的发病机制有了更深入的理解。
结 语
这项研究也为我们理解细胞衰老机制提供了新的视角。细胞衰老与多种疾病的发生发展密切相关,包括神经退行性疾病、心血管疾病等。通过深入研究DNA2与细胞衰老的关系,我们或许能够找到延缓细胞衰老、预防相关疾病的方法。
随着生物技术的不断发展,我们有理由相信,在不久的将来,我们将对DNA2的功能有更全面、深入的认识,并且能够利用这些知识为人类健康事业做出更大的贡献。DNA2这个神秘的“分子卫士”,将在生命科学的舞台上继续绽放光彩,为我们揭示更多生命的奥秘
参考文献
1:DNA2 enables growth by restricting recombination-restarted replication
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

