
当衰老的免疫细胞遇见再生的希望,疫苗保护力竟可飙升400%——这并非科幻情节,而是中山大学科学家在《细胞与分子免疫学》揭开的生命奇迹。
2026年1月9日,一项由中山大学项鹏、陈小湧、李伟强和陈莉莉等发表于《细胞与分子免疫学》的重要研究,为破解这一难题带来了全新的曙光。研究团队发现,通过静脉输注间充质干细胞(Mesenchymal Stromal Cells, MSCs),能够显著逆转老年小鼠的免疫衰老状态,并大幅提升后续流感疫苗的免疫效果和实际保护力。更令人振奋的是,这一效应在老年食蟹猴模型中也得到了验证。这不仅为开发增强老年人疫苗应答的新策略提供了扎实的科学依据,也让我们对干细胞如何调控免疫系统有了更深刻的认识。

MSCs修复了老年小鼠脾脏基质细胞中与年龄相关的缺陷
研究人员发现与年轻小鼠(2-3个月)相比,老年小鼠(18-21个月)的脾脏略有下降(扩展数据图1A-C)。老年脾脏中脾基质细胞的频率和数量显著减少(扩展数据图1D-F),免疫荧光染色也证实了这一点(扩展数据表1G,H)。此外,免疫荧光(扩展数据图1I)和苏木精和伊红(H&E)染色(扩展数据表1J)显示,老年脾脏的白髓区域结构紊乱,大小显著减小。总的来说,这些结果表明,衰老会导致脾脏基质细胞减少,并损害脾脏的微结构
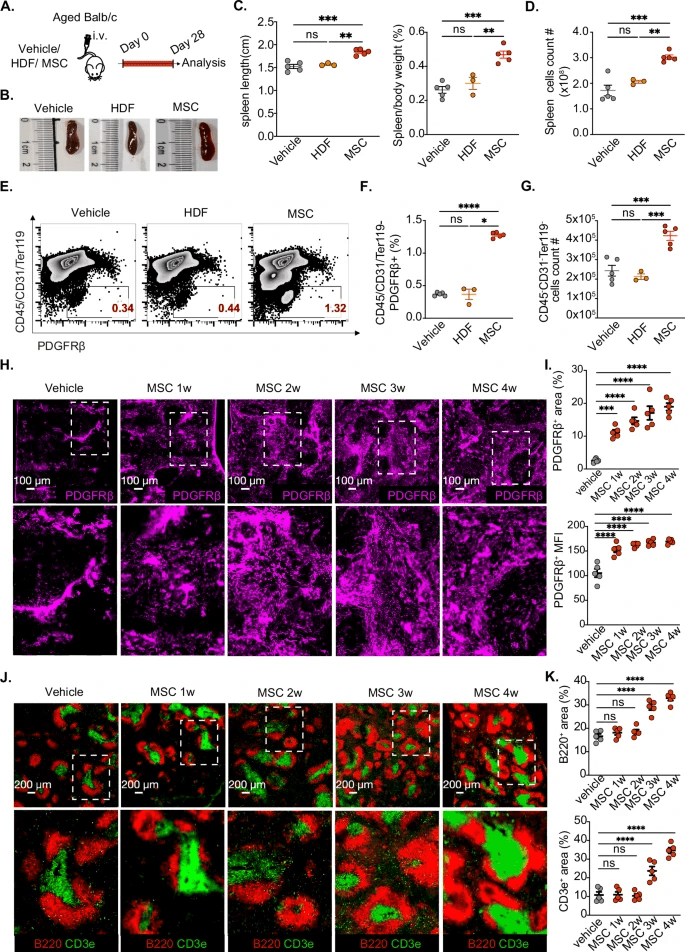
发现表明,外源性MSCs可以重塑衰老脾脏中的基质细胞网络,从而恢复免疫细胞群和微结构的完整性。
如图2所示,对年龄在18-21个月的小鼠施用MSCs。治疗后28天,用完全弗氏佐剂(CFA)中的卵清蛋白(OVA)对小鼠进行腹膜内免疫,14天后用不完全弗氏助剂(IFA)中的OVA进行加强免疫。虽然OVA免疫后对照组的脾脏变化很小,但MSC治疗组的脾脏明显增大,特别是在OVA免疫后(图2B-E)。与对照组相比,MSC给药导致花生凝集素(PNA)阳性荧光区域(GC区域)扩大,提供了GC形成增强的额外证据(图2H,I)。此外,研究发现Tfh细胞定位在GC内以支持GC反应,进一步支持OVA免疫后MSC给药后GC形成的增强(扩展数据图4A)。
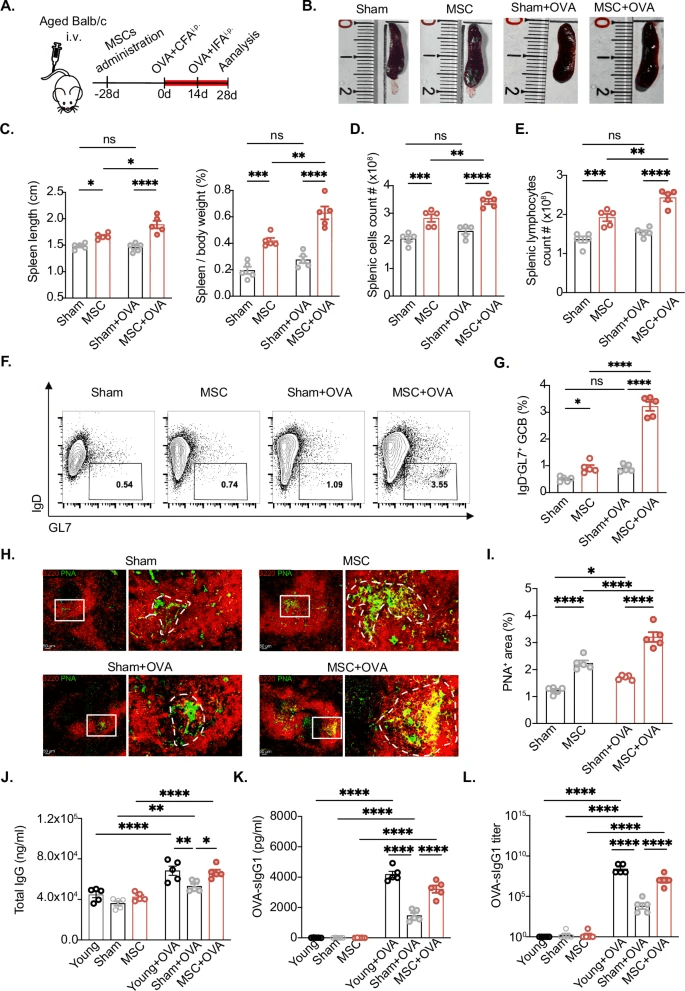
OVA免疫后,在年轻、老年和MSC处理的小鼠血清中检测到总IgG水平显著升高,证实了所有组的免疫激活。与GC形成的结果一致,老年小鼠的总IgG水平明显低于年轻小鼠,MSC干预导致IgG产量明显增加(图2J)。重要的是,对OVA特异性IgG水平的进一步分析显示,年轻小鼠在免疫后的抗体反应比老年小鼠更为强烈(图2K,L)。
大多数针对老年人的疫苗提供的保护有限,导致感染后发病率和死亡率增加,如甲型流感病毒感染。为了解决这个问题,研究评估了MSCs给药对疫苗疗效和老年小鼠流感感染防护的影响。接种疫苗前四周,给老年小鼠注射MSCs(图3A)。为了将临床前发现与临床相关性联系起来,用四价流感疫苗(QIV,目前人类疫苗接种的临床标准)对小鼠进行免疫接种,其接受间隔14天的两次剂量。与OVA免疫结果一致,MSC治疗组表现出明显的脾脏增大,同时脾脏淋巴细胞和生发中心B细胞增加(图3B-F),表明疫苗诱导的免疫反应比对照组更强烈。免疫荧光染色进一步证实,MSC处理的小鼠脾脏生发中心的形成增加(图3G)。此外,MSC治疗组在接种疫苗后的总IgG水平比对照组有更明显的增加(图3H)。随后的血凝抑制(HI)检测显示,MSC治疗组的流感疫苗血清抗体滴度明显高于对照组(图3I)。这些发现表明,MSC给药显著增强了老年小鼠对流感疫苗接种的体液免疫反应。
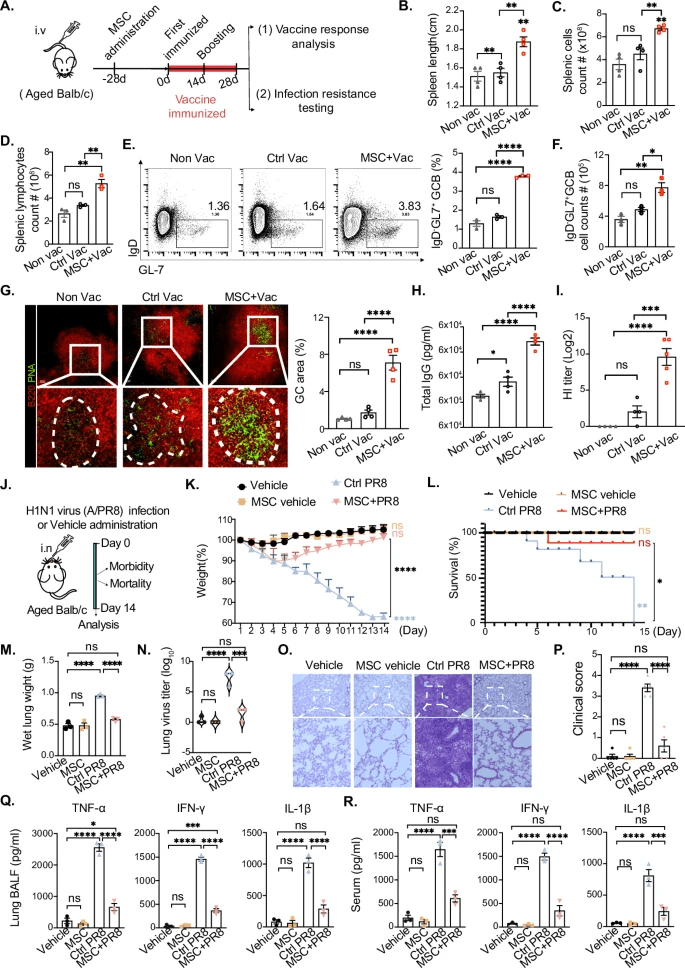
在流感病毒感染后,MSC治疗的小鼠在肺组织和体循环中的促炎因子水平显著降低(图3Q,R)。这些发现强调了MSCs在缓解与年龄相关的体液免疫下降、增强疫苗反应性以及为老年人提供有效的感染防护方面的潜力。
如扩展数据图5所示,数据表明MSC增强的疫苗反应在脾切除术后完全消除(扩展数据图5B-D)。这些发现从机制上证实了脾脏是一个非冗余的淋巴生态位,协调MSC介导的免疫增强。
MSCs未能重建这些小鼠的T和B细胞微环境(扩展数据图6B),因此导致MSCs给药后无法提高OVA诱导的抗体水平(扩展数据表8A-H)。此外,在MSC注射后的早期阶段(图4A),检测到脾细胞的增殖(Ki-67表达)显著增加(扩展数据图9A-C),特别是在CD45-亚群中(扩展数据表9C,D)。这一观察结果进一步得到了以下发现的证实,即脾脏基质细胞的重塑先于T细胞和B细胞的变化(图1J-K)。综上所述,这些结果表明,脾基质细胞可能是MSC介导干预的先决条件细胞靶群。
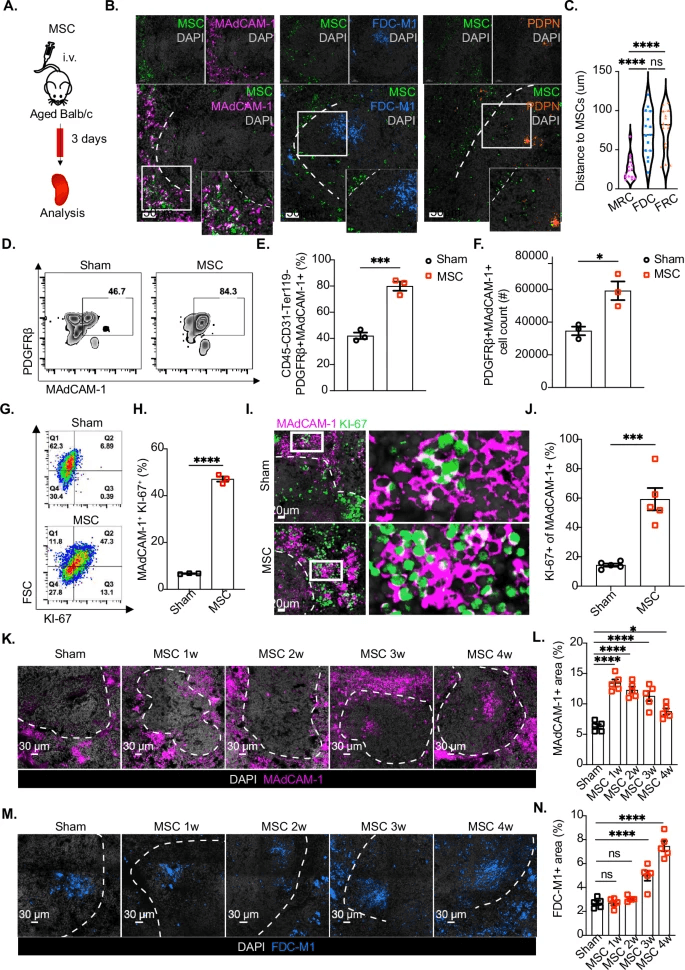
脾脏中有三组主要的基质细胞,即边缘网状细胞(MRC)、滤泡树突细胞(FDCs)和成纤维网状细胞(FRCs)。我们发现许多间充质干细胞分布在脾脏内,主要局限于由MRC支撑的边缘区,MRC表达粘附分子MAdCAM-1(图4B,C)。
MSCs促进老年脾脏中MRC的增殖,从而增加FDCs的数量,这对GC促进和疫苗反应至关重要。
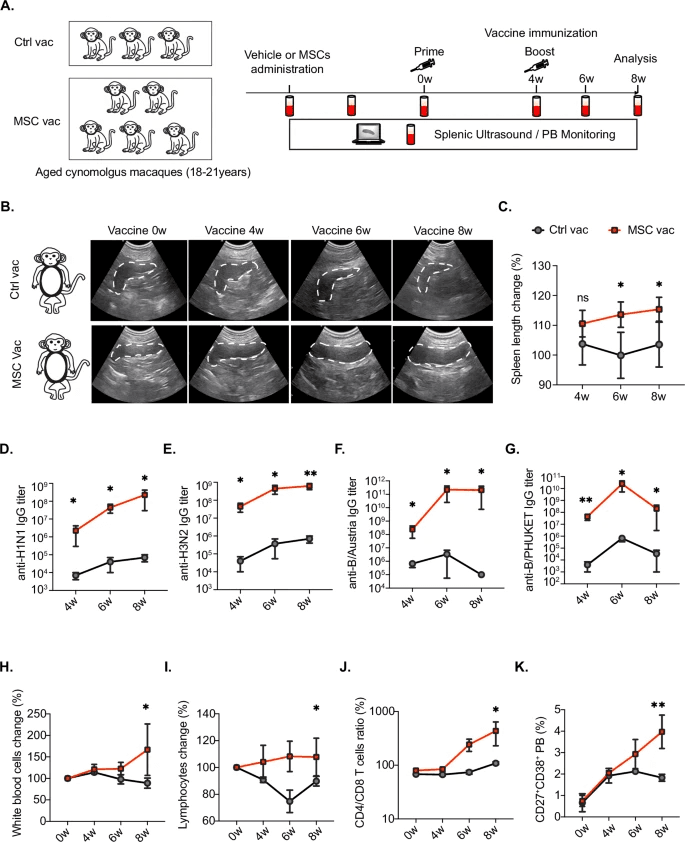
为了评估基于MSC的干预措施对人类疫苗接种策略的转化潜力,使用老年食蟹猴(17-20岁,表1)建立了一个流感疫苗接种模型,这是一种在免疫系统特征方面与人类非常相似的物种。在MSC给药前收集基线数据,包括血液样本和腹部脾脏超声数据。随后,将MSC或PBS(载体对照)静脉注射给老年食蟹猴,并进行每日健康评估(图6A)。MSC或载体给药9周后,所有受试者均接受了0.5 mL四价流感疫苗(QIV),其中含有15 每种流感病毒株(H1N1、H3N2、B/维多利亚流感谱系和B/山形流感谱系)的HAµg。血液分析显示,免疫后白细胞和淋巴细胞的相对比例增加,持续时间长达8周(图6H,I)。MSC输注组还表现出淋巴细胞计数、CD4/CD8比值和CD19+CD27+CD38+B细胞(浆母细胞)升高,进一步证实了良好的疫苗反应(图6J,K)
研究表明外源性MSCs增强了老年小鼠和猴子接种疫苗后的免疫反应和特异性抗体的产生,并强调了使用脾脏MRC作为恢复脾脏结构和增强老年人免疫反应的有前景的策略。这些结果显著扩展了对外源性MSCs作用机制的理解,除了它们对免疫细胞的直接影响外,还调节内源性基质细胞的数量和功能,维持免疫稳态。
免疫衰老

老年人免疫功能的衰退显著增加了其感染风险。65岁及以上成年人因严重流感和肺炎导致的死亡率明显升高,该年龄段住院患者中超过60%死于流感感染。疫苗接种是预防流感的首选方案,因为感染后抗病毒治疗在降低死亡率方面效果有限。然而,疫苗接种的有效性和实际保护效力在老年人群中显著降低,这与免疫功能逐渐衰退的年龄相关免疫缺陷特征密切相关。
免疫衰老:疫苗保护的“隐形杀手”
随着机体衰老,免疫系统逐渐陷入“疲惫状态”:
T细胞耗竭:对抗病原体的主力军反应迟钝
抗体生产线萎缩:生发中心功能衰退导致抗体产量锐减
炎症风暴隐患:促炎因子与抑炎因子平衡打破
这正是老年人接种疫苗后保护率不足30%的关键原因,直到间充质干细胞(MSCs)带来破局曙光。
作用机制解密:干细胞的三重赋能
01微环境修复
MSCs分泌的TGF-β、IL-10等因子重塑淋巴组织,重建适合免疫细胞生长的“生态家园”
02线粒体移植
通过隧道纳米管向衰老免疫细胞输送健康线粒体,重振细胞能量工厂
03表观遗传调控
调控DNA甲基化模式,逆转免疫细胞衰老相关基因表达
结束语
“MSCs就像免疫系统的‘充电宝’,不仅重启老化电池,还能升级系统版本。”——研究团队负责人比喻道科学家在实验室里唤醒衰老小鼠的免疫青春时,我们隐约看见这样的未来——百岁老人接种一针疫苗,获得的保护力堪比青年。这项突破不仅关乎疫苗效果,更在重新定义人类对抗衰老的边界。
参考文献
1:Mesenchymal stromal cells counteract with age-related immune decline and enhance vaccine efficacy by modulating endogenous splenic marginal reticular cells in elderly models
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

