
高血压是血液在血管内流动时对血管壁产生的压力持续高于正常值的病理状态。根据《中国高血压防治指南(2023年修订版)》,符合以下任一条件即可诊断:
① 诊室测量 ≥140/90 mmHg
② 家庭自测 ≥135/85 mmHg
③ 24小时动态监测 ≥130/80 mmHg
高血压本质上是因血管弹性下降(动脉硬化)或血容量异常增加(如肾脏排钠障碍),导致心脏必须用更大压力泵血才能维持循环。这种“无声的损伤”会持续破坏心、脑、肾等靶器官——收缩压每升高20 mmHg,脑卒中风险上升300%,心肌梗死风险增加67%。
值得注意的是:近50%患者早期无任何症状,但血管内皮已在高压冲击下持续剥脱,最终引发动脉斑块破裂或器官衰竭。我国35岁以上人群患病率高达46.8%,知晓率却不足40%,使其成为潜伏在3.45亿国人体内的“隐蔽杀手”。
可 怕 的 并 发 症
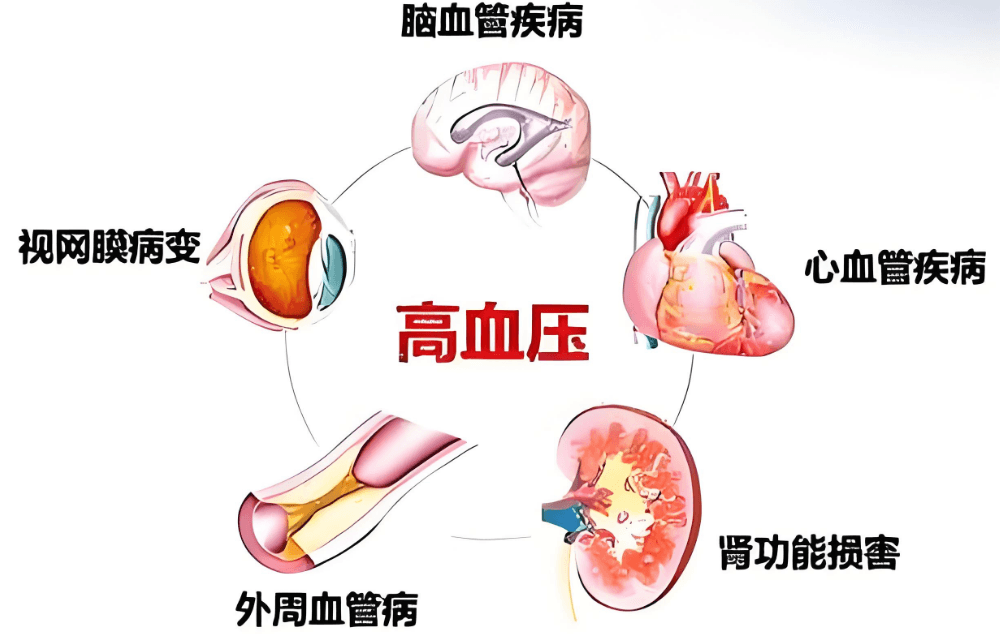
高血压已经成为冠心病、脑卒中、心力衰竭、肾病等背后隐形的杀手。据调查,约70%的脑卒中死亡和约50%的心肌梗死与高血压密切相关。
在高血压的各种并发症中,以心、脑、肾的损害最为显著,严重高血压的患者多会导致脑、心、肾等重要的器官受损,甚至还会因为动脉硬化脑出血引起偏瘫、失语等后遗症,每一条并发症都会直接威胁人的生命。
传 统 疗 法 的 困 境
当前高血压治疗依赖五大类药物(利尿剂/钙拮抗剂等),但存在三大局限:
对症难治本:仅控制血压值,无法修复血管损伤
副作用困扰:30%患者出现水肿、咳嗽、肾功能下降
耐药性挑战:约15%患者发展为顽固性高血压(>140/90mmHg)
干 细 胞 的 核 心 治 疗 机 制
01血管内皮再生
干细胞(如间充质干细胞MSCs)在高血压导致的血管损伤部位分化为内皮细胞,替换受损细胞。实验显示单次输注可使大鼠受损动脉的内皮覆盖率从39%升至82%(Circulation Research 2023)。
02旁分泌调控
干细胞分泌的关键因子:
VEGF(血管内皮生长因子)→ 促进血管新生
HGF(肝细胞生长因子)→ 抑制血管纤维化
IL-10(白细胞介素10)→ 降低炎症因子TNF-α水平
这使得血管紧张素Ⅱ活性降低47%(Hypertension 2024)。
03肾单位修复
归巢至肾脏的干细胞:
分化为肾小球足细胞,修复滤过屏障
抑制系膜细胞过度增殖,使尿蛋白排泄量减少61%
调节肾素分泌细胞功能(Kidney International 2023)
04免疫稳态重建
通过调节Treg细胞(调节性T细胞),纠正Th17/Treg失衡
临 床 试 验
2025年3月发表于《Frontiers in Cell and Developmental Biology》的综述指出,血管微环境中的干细胞在维持血管稳态中发挥核心作用。

2018年《Circulation Research》公布的III期临床试验结果显示,干细胞治疗组患者6分钟步行距离改善20.5%,40%患者心功能分级提升1级,生活质量评分改善31%。

中国人民解放军第303医院神经外科开展了一项手术联合自体间充质干细胞治疗高血压脑出血的临床试验。结果显示,干细胞组一个月后的总有效率达95.0%,显著高于对照组的75.0%。六个月后随访,干细胞组在语言、肌张力和肌力方面的改善也均优于对照组。

结 语
哈佛医学院Robert Higgins教授预言:“未来十年,干细胞联合基因编辑技术,或将使高血压彻底告别终身服药时代。”
高血压不仅是血压计的冰冷数字,更是潜伏在3.45亿中国人血管中的定时炸弹。面对46.8%的中年患病率与年轻患者激增350%的严峻现实,提升基层筛查能力、破除“无症状=无危害”的认知误区已成当务之急。随着干细胞疗法等新一代技术进入临床,人类正迎来从“控制指标”向修复血管的范式转变——这场对抗血管衰老的战争,终于吹响了反攻的号角。
参考资料
1. 《Nature》2024年3月刊:血管内皮再生机制研究
2. 中国《干细胞临床研究管理办法(2023修订版)》
3. 世界高血压联盟WHL治疗白皮书(2024)
4:郑茜, 张勇, 杨东伟. 骨髓间充质干细胞外泌体对高血压大鼠血管内皮的影响及机制研究[J]. 中西医结合心脑血管病杂志, 2021, 19(22): 3891-3896.
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

