
背景: 全球约35亿人患有口腔疾病,其中中国龋齿和牙周病患病率超过70%,但疗法率不足15%。预计到2025年,全球口腔医疗市场规模将突破1800亿美元,中国占比将达22%。研究显示,84%的临床诊断为不可逆性牙髓炎的牙齿在组织学上与之相符,然而仍有16%的牙齿在组织学上表现为正常或轻微炎症。因此,保护口腔健康已成为迫切的任务。
原理:牙髓是位于牙齿髓腔内的疏松结缔组织,主要由血管和神经构成,承担着牙齿的营养供应和感觉传导功能。由于其解剖结构特殊,血液供应单一且缺乏侧支循环,容易因龋病或创伤等刺激引发炎症反应,且难以通过自身防御系统消除感染,常导致不可逆性牙髓坏死。此外,牙髓不同区域由不同类型的细胞组成,坏死后难以再生包含多种细胞的牙髓牙本质复合体。
临床上常用方法
目前,临床上治疗不可逆性牙髓坏死最常用的方法是根管治疗,通过清除感染的牙髓组织并填充根管来控制病情。然而,根管治疗存在诸多弊端,比如会出现冠部微渗漏,进而导致继发感染,还会使牙齿机械性能下降、脆性增加,牙齿的营养和防御功能也会随之丧失。
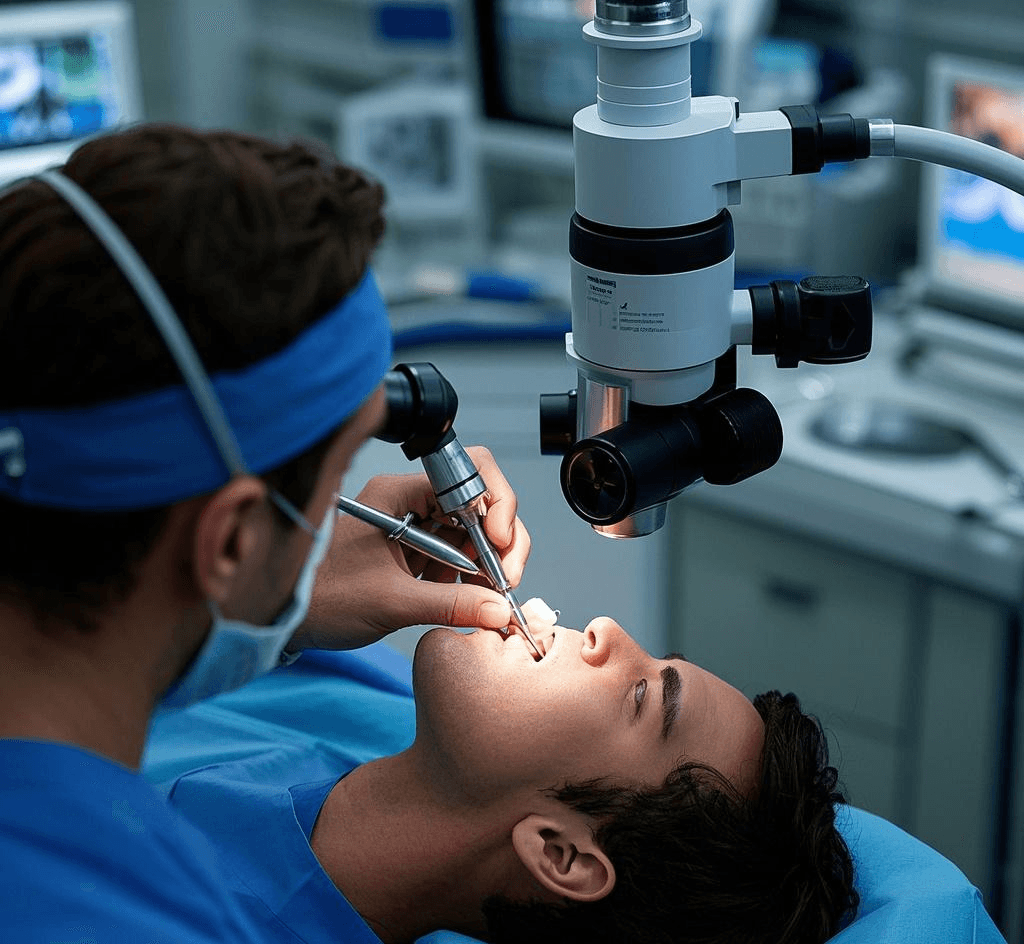
随着细胞学、生物学和工程学技术的发展,牙髓组织工程成为口腔医学的研究热点。该技术将细胞、活性因子和生物材料相结合,在体外构建活性牙髓组织以替代坏死组织,实现牙髓功能的重建。其中,利用新技术诱导牙髓组织内多种细胞形成,重建具有生物学活性的牙髓牙本质复合体,已成为改善不可逆性牙髓坏死的重点研究方向。
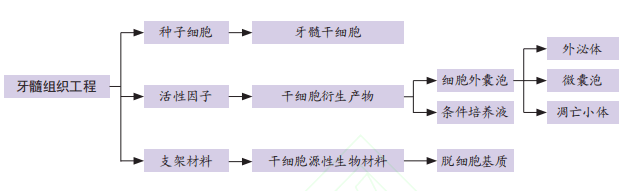
牙髓干细胞作为牙髓组织工程的关键种子细胞,具有取材简便、微创且无伦理问题的优点,主要来源于成人正畸牙、埋伏牙和第三磨牙等牙齿相关组织。这些干细胞具有自我更新和多向分化潜能,能在体外分化成牙本质、血管和神经等组织,并在动物体内形成血管化的牙髓牙本质复合体,广泛应用于牙髓再生领域。近年来,牙髓干细胞及其衍生物在牙髓再生治疗中取得显著进展,为年轻患者的牙齿修复提供了新的治疗前景。
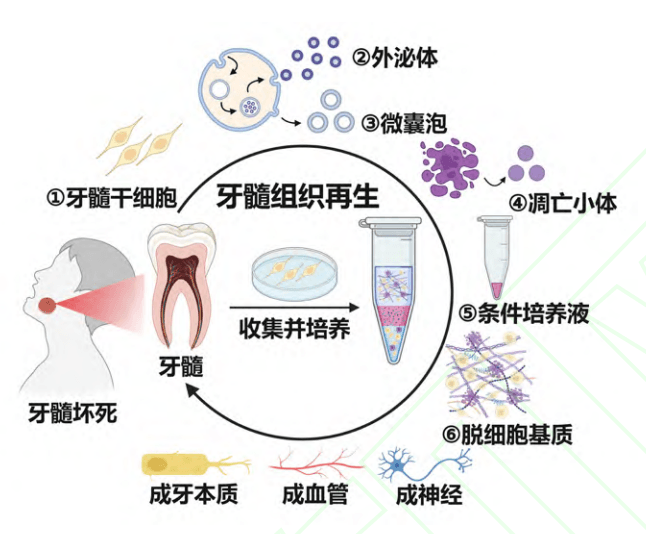
图1|牙髓干细胞及其衍生产物在牙髓再生中的作用
如图1显示,牙髓干细胞源性衍生产物如细胞外囊泡(extracellular vesicles,EVs),条件培养液(conditioned medium,CM)以及脱细胞基质(decellularized extracellularmatrix,dECM)等,含有大量细胞活性因子,具有促进细胞增殖、分化以及组织修复的潜能,在牙髓损伤修复和再生领域也广泛研究。此综述将深入探讨牙髓干细胞及其衍生产物在牙髓组织工程中的应用与进展,通过对一系列研究成果的综合分析,有望为不可逆性牙髓炎提供新的疗法策略,为牙髓组织工程未来的前景带来创新性的发展。
牙髓干细胞在牙髓组织工程中的应用
1.定义及特征
牙髓干细胞是来源于牙髓组织的多能干细胞,具有易获取、无伦理问题和免疫排斥反应低的优点,主要通过酶消化法从正畸拔除牙齿、埋伏牙和第三磨牙等组织中提取。这些干细胞具有多向分化能力和高度增殖潜力,可以分化为多种细胞类型,如成牙本质细胞、成骨细胞、血管内皮细胞和神经细胞。同时,牙髓干细胞通过旁分泌机制释放多种生长因子,促进血管生成和神经再生,成为牙髓再生的关键细胞来源。
2.在牙髓再生中的应用
在牙髓再生过程中,提高牙髓干细胞活性并促进其向成牙本质细胞和血管内皮细胞分化,是恢复牙髓组织结构和功能的关键方法。近年来,工程化干细胞被广泛应用于牙髓再生治疗,通过细胞因子调控、生物材料支持、物理条件调节和基因工程编辑等手段,显著提升牙髓干细胞活性,促进其分化,促进牙髓组织修复与再生。多种技术共同作用,精确调控细胞的增殖与分化,增强再生效果。
(1)活性:为了提高牙髓再生效果,研究者们通过多种工程化干预方案增强和维持牙髓干细胞的活性,如增殖、迁移、分化、免疫调节等。这些措施为血运重建和牙髓-牙本质样结构的形成奠定基础。具体方法包括使用不同物质(如大麻二酚、姜黄素纳米颗粒、等离子体纳米材料等)或生物材料(如自体牙髓干细胞与血小板纤维蛋白基质、磁性纳米颗粒等),通过调节细胞因子、miRNA、免疫活性和干细胞极性,促进牙髓干细胞的活性、定向分化及组织再生。
(2)向成牙本质细胞分化:牙髓-牙本质复合体的重建是牙髓再生的关键,牙髓干细胞在不同信号通路的调控下能够分化为成牙本质细胞,促进复合体再生。研究表明,BTB和CNC同源、Ras-ERK/AKT、蛋白激酶B、ERK、核糖体蛋白S6等信号通路参与了这一分化过程。此外,镁离子和特定生物材料的应用也促进了该过程。干细胞与支架材料的联合应用在体外和体内实验中展示了显著的再生效果,为牙髓再生提供了有效的治疗策略。相关文献见表 1.
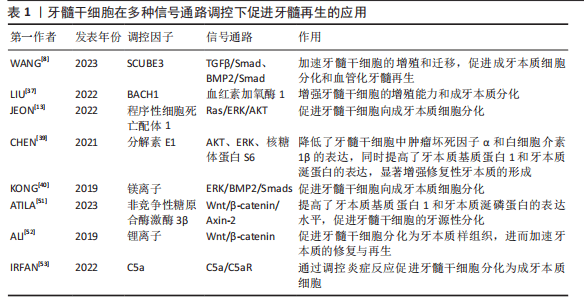
表注:SCUBE3为信号肽·CUB-EGF结构域含蛋自3,TGFβ为转化生长因子阝,Smad为Sma 和 Mad 相关蛋白,BMP2为骨形态发生蛋白 2,BACH1为 BTB和CNC 同源1,Ras为小鼠肉瘤病毒相关GTP 声,ERK为细胞外信号调节激酶,AKT 为蛋白激酶 B,Wnt 为翼状/整合蛋白,β-catenin 为阝- 连环蛋白,Axin2 为轴突蛋白 2,C5a为补体 5a,c5aR 为补体5a 受体。
(3)向血管内皮细胞分化:在牙髓重建过程中,新生血管对周围组织的营养支持至关重要,并促进牙髓干细胞向血管内皮细胞分化。研究者通过细胞共培养、引入生长因子和活性材料等方式,提升了牙髓干细胞的血管生成能力。相关研究表明,内皮分化培养基、血小板裂解液、骨形态发生蛋白和铜离子等因素显著促进牙髓干细胞的血管生成,有助于牙髓样组织的形成。此外,干细胞疗法在临床前研究中展现出良好的安全性与有效性,促进牙髓再生,并通过新型基因载体技术进一步增强血管生成潜力。
细胞外囊泡在牙髓组织工程中的应用
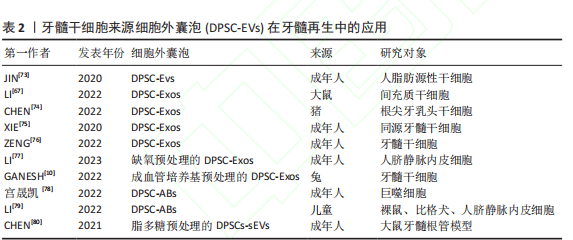
1.定义及特征:牙髓干细胞来源的细胞外囊泡是由牙髓干细胞分泌的纳米级囊泡,具有高度稳定性和生物相容性。根据囊泡的大小和形成机制,细胞外囊泡可分为外泌体、微囊泡和凋亡小体。牙髓干细胞因其基因工程可行性,成为细胞外囊泡的理想来源。通过离心收集牙髓干细胞上清液,可以得到富含蛋白质、脂质及RNA等活性因子的细胞外囊泡。由于其低免疫排斥风险和较高的基因工程改造可行性,牙髓干细胞来源的细胞外囊泡在牙髓组织工程中被视为一种具有潜力的无细胞疗法。相关文献见表2.
2.在牙髓再生方面的应用促进成牙本质分化:牙髓干细胞来源的细胞外囊泡在牙髓再生中发挥重要作用,能够通过调控多种信号通路促进成牙本质、血管和神经的分化。它们携带的活性因子和miRNA调控干细胞向成牙本质细胞、成骨细胞、血管和神经细胞的分化,推动牙髓组织修复和再生。此外,脂多糖预处理的牙髓干细胞分泌的外泌体在促进血管、神经及牙本质再生方面展现出更强的能力。研究还表明,年轻与老年供体来源的细胞外囊泡在再生能力上存在差异,年轻供体的外泌体在促进血管生成和神经再生方面更为显著,具有更大的治疗潜力。
牙髓干细胞的临床进展
2013年,中国第四军医大学已开展80例临床试验,以来自于脱落乳牙的自体干细胞,进行牙髓坏死的再生治疗,并取得良好效果。

2018年8月,来自中国第四军医大学的研究人员和美国宾夕法尼亚大学的研究人员发表于《Science Translational Medicine》一项临床试验的结果显示,对于患有牙髓损伤的儿童来说,有一种更有安全有效的治疗途径,即用患者自体人乳牙髓干细胞(hDPSC)移植使牙髓再生。

总结与期望
牙髓组织工程面临多重挑战,尽管牙髓干细胞在牙髓损伤后的再生修复中具有潜力,但其应用仍受到干细胞特性限制。当前研究重点包括优化支架材料和细胞外基质、提高干细胞活性和应用基因编辑技术。然而,临床应用中仍面临免疫原性、稳定性和活性因子递送等挑战。未来研究应深入了解牙髓干细胞衍生物机制,开发高效的活性因子递送系统,并解决批次差异性、生产成本等技术难题。同时,个性化治疗和精准医学将是未来牙髓再生领域的重要发展方向。
参考文献
[1]徐海超,罗丽花,潘乙怀.牙髓干细胞及衍生产物在牙髓再生中的应用与进展[J/OL].中国组织工程研究,1-9[2025-02-24].http://portal.sclib.cn/interlibSSO/goto/11/+jmr9bmjh9mds/kcms/detail/21.1581.R.20250221.1008.002.html.
[2] SUIB, CHEN C, KoU X,et al. Pulp Stem Cell-Mediated Functional Pulp Regeneration. J DentRes. 2019;98(1):27-35.
[3] ReferencesLIANG Q, LANG C, LlUX, et al. Vascularizeddental pulp regeneration using cell-ladenmicrofiber ageregates. 」 Mater Chem B. 2022;10(48):10097-10111.
免责声明:本文旨在科普相关知识,不作为医疗指导意见。
编辑|LiYe.ZG
审核|Geng.ZG

