
癌症,这个令人谈之色变的 “健康杀手”,如今正以前所未有的速度威胁着人类的生命健康。据相关数据显示,全球每年新增癌症病例数以百万计,在中国,癌症的发病率和死亡率也都处于高位。肺癌、乳腺癌、胃癌等常见癌症类型,如同阴霾笼罩着无数家庭,给患者带来身体与精神的双重折磨,也给社会造成沉重负担。

近年来,随着医学研究的深入,科学家们惊喜地发现,通过将 NK 细胞与胎盘干细胞巧妙共培养,能够极大地激发 NK 细胞的抗癌潜能,使其在短短 24 小时内消灭近 90% 的癌细胞。
抗癌先锋 NK 细胞
NK 细胞,全称为自然杀伤细胞(Natural Killer Cell),是人体免疫系统中的一支 “特种部队”。它隶属于淋巴细胞家族,却有着与众不同的特性。与 T 细胞、B 细胞等免疫细胞需要经过复杂的抗原识别、呈递等过程才能发挥作用不同,NK 细胞具有天然的免疫活性,能够迅速对 “异常细胞” 做出反应,在机体的免疫防御体系中占据着至关重要的前沿阵地。

NK 细胞的抗癌机制堪称精妙绝伦。一方面,它具备强大的直接杀伤能力,通过释放穿孔素和颗粒酶等细胞毒性物质,在癌细胞的细胞膜上 “打孔”,进而降解癌细胞内部的蛋白质,致使癌细胞凋亡瓦解;另一方面,NK 细胞还能分泌多种细胞因子,如干扰素 -γ(IFN-γ)、肿瘤坏死因子 -α(TNF-α)等,这些细胞因子不仅可以直接抑制癌细胞的生长、增殖,还能激活机体其他免疫细胞,如 T 细胞、巨噬细胞等,协同作战,共同营造出一个对癌细胞极为不利的免疫微环境,全方位地遏制癌症的发展。
然而,在癌症治疗的实战中,NK 细胞却面临着诸多困境。肿瘤微环境,这个癌细胞赖以生存的 “堡垒”,充满了重重挑战。其中,免疫抑制分子的大量分泌,使NK 细胞活性受到严重抑制;营养物质的匮乏以及代谢废物的堆积,让 NK 细胞的增殖和杀伤能力大打折扣;此外,癌细胞还会通过伪装,下调自身表面的抗原表达,让 NK 细胞难以识别。这些难题,都使得 NK 细胞在抗癌征程中变得异常艰难。
胎盘干细胞的独特优势
胎盘干细胞,源自新生儿娩出后的胎盘组织,是一类具有非凡潜力的干细胞。胎盘干细胞具有多潜能分化的神奇特性,在特定的诱导条件下,它可以分化为成骨细胞、软骨细胞、脂肪细胞、神经细胞等多种细胞,为组织修复与再生提供了源源不断的 “种子细胞”,无论是骨折后的骨愈合、关节软骨损伤的修复,还是神经系统疾病的治疗,都展现出了巨大的应用潜力。

更为关键的是,胎盘干细胞具有低免疫原性的突出优势,这意味着它在进入异体体内后,引发免疫排斥反应的风险极低。相较于其他来源的干细胞,胎盘干细胞表面的主要组织相容性复合体(MHC)分子表达水平较低,使得它能够巧妙地避开受体免疫系统的 “攻击”。
凭借这些独特优势,胎盘干细胞可用于治疗各类难治性疾病,如糖尿病、心肌梗死、肝硬化等,它还在免疫调节治疗方面展现出卓越疗效,为自身免疫性疾病、移植物抗宿主病等棘手病症提供了全新的治疗思路。
共培养的神奇反应
在这项开创性的研究中,科学家们精心设计了实验。他们从人类足月胎盘的母体蜕膜中提取出间充质干细胞(DBMSCs),与此同时,获取具有代表性的 NK 细胞。随后,将这两种细胞置于特定的共培养体系中,模拟体内微环境,在适宜的温度、湿度以及营养条件下,让它们 “相互交流”。
实验结果令人惊叹不已。研究人员通过先进的分子生物学检测技术发现,NK 细胞的多种分子表达发生了显著变化。其中,NKp30、NKp44、NKp46 等活化分子的表达水平大幅提升,使其能够更敏锐地识别癌细胞,并且在接触癌细胞的瞬间,迅速激活杀伤机制,对癌细胞发动更为猛烈的攻击。
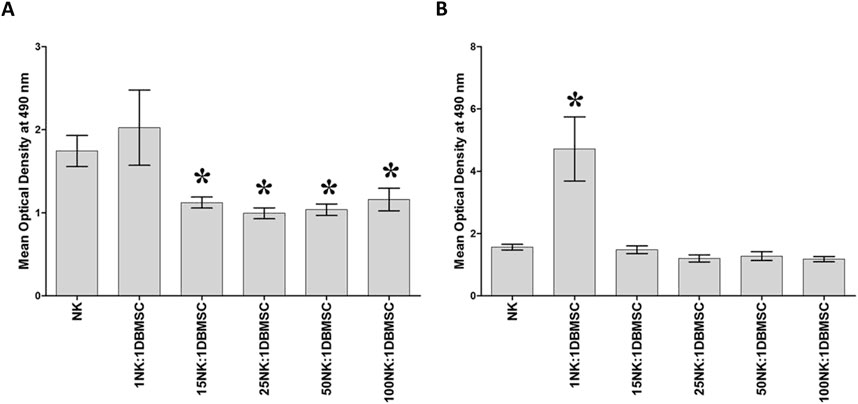
当活化的 NK 细胞与乳腺癌细胞(MCF-7)共同培养时,其杀伤性能得到了切实验证。在设置 NK 细胞与癌细胞比例为 10:1 的实验场景下,未经过 DBMSCs 共同培养的 NK 细胞,对癌细胞的杀伤率仅徘徊在 30% 左右。与之形成鲜明对比的是,与 DBMSCs 完成共培养流程后的 NK 细胞,展现出令人惊叹的实力,在短短 24 小时内,就能够将接近 90% 的癌细胞清除。
进一步将实验条件调整为,把经 DBMSCs 预先处理的 NK 细胞与 MCF-7 按照 1:1 的较低比例进行共培养,结果发现,其对癌细胞增殖的遏制成效依然极为突出 —— 癌细胞的增殖速率大幅放缓,增殖率下降幅度径直达到 60%。
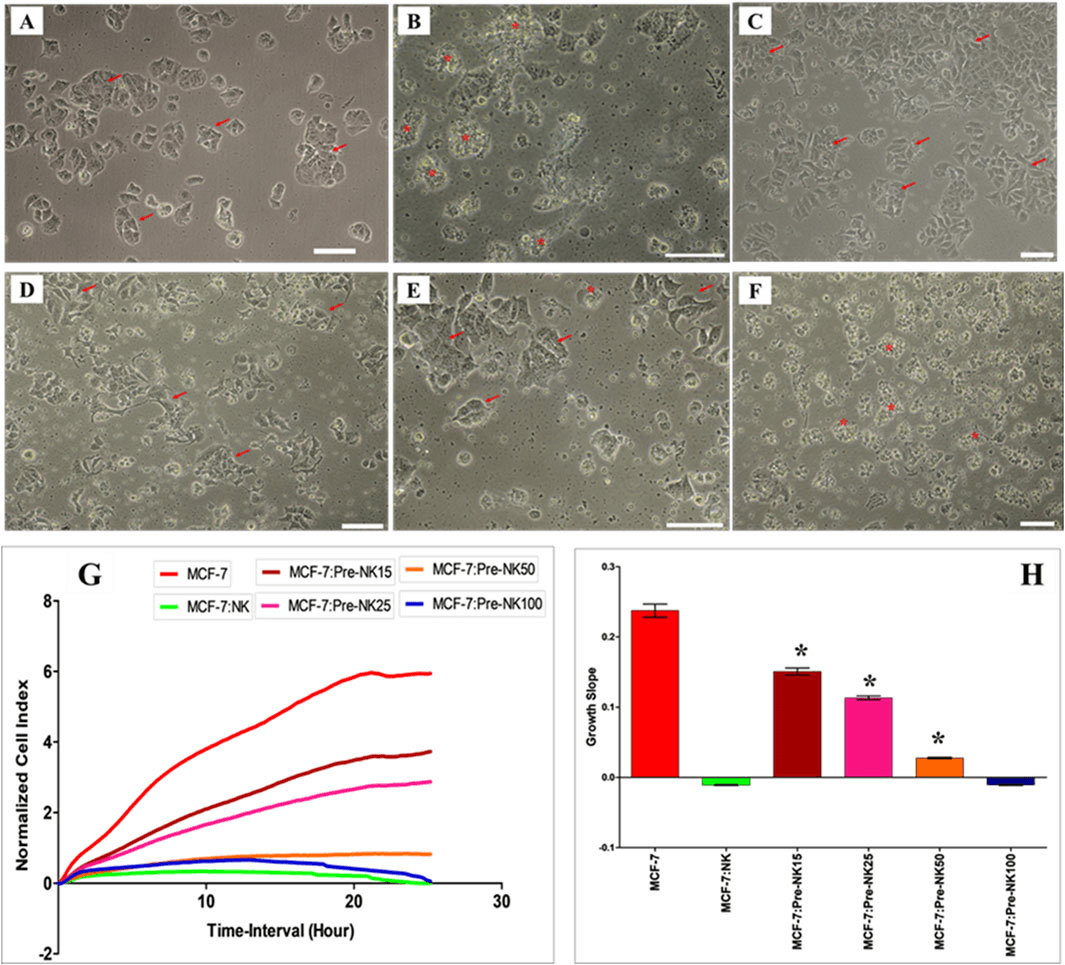
综合上述一系列实验成果,可以看出,干细胞在提升 NK 细胞抗癌能力方面,扮演着极为关键的角色。形象地说,干细胞宛如为 NK 细胞的抗癌征程安装了强劲的助推引擎,极大地增强了 NK 细胞对抗癌症的效力 。
深入探究其背后的原理,一方面,DBMSCs 能够分泌多种细胞因子,如白细胞介素 - 18(IL-18)、干扰素 -γ(IFN-γ)等。这些细胞因子不仅可以直接作用于 NK 细胞,激活其内部的信号传导通路,上调活化分子的表达,还能增强 NK 细胞的代谢活性;
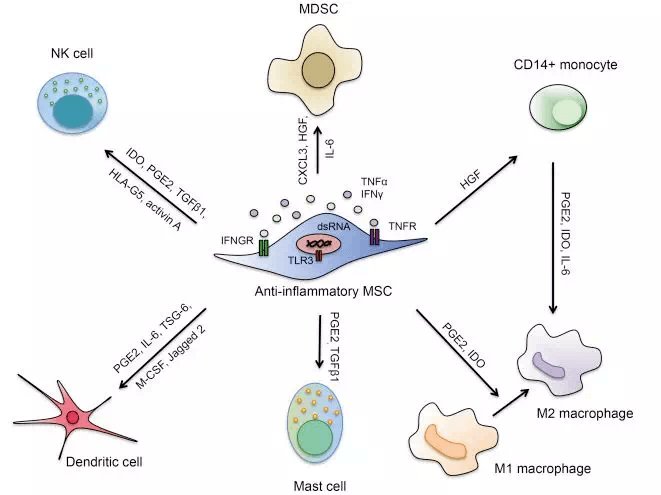
另一方面,DBMSCs 凭借自身独特的免疫调节特性,重塑了肿瘤微环境。它能够抑制肿瘤微环境中的免疫抑制分子,如转化生长因子 -β(TGF-β)、程序性死亡配体 - 1(PD-L1)等的分泌,打破癌细胞对 NK 细胞的 “禁锢”,让 NK 细胞得以在肿瘤组织中自由穿梭,全力施展抗癌本领。
结语
干细胞治疗作为医学领域的一项前沿技术,为众多疾病的治疗提供了新的希望和可能。然而,其疗效与安全性高度依赖于患者的准备、选择正规机构以及明确的治疗需求与预期。在未来的日子里,让我们共同期待干细胞治疗为更多患者带来生命的奇迹与希望。
参考文献
Abdulaziz Almutairi,et,al.Human decidua basalis mesenchymal stem/stromal cells enhance anticancer properties of human natural killer cells, in vitro.
免责声明:本文旨在科普相关知识,不作为医疗指导意见。
编辑|Lin.ZG
审核|Geng.ZG

