
在日常生活中,骨折作为一种频发的意外损伤,不仅给患者的身体带来深重的痛苦,还极大地影响了他们的日常生活便利性。然而,随着医学研究的不断深入,一个曾经相对陌生的概念——外泌体,悄然步入了骨折治疗的舞台,为这一传统领域注入了新的活力与希望。外泌体,作为细胞间交流的桥梁,近年来在骨折治疗,引起了广泛的关注与探讨。那么,骨折与外泌体之间究竟存在着怎样神秘而奇妙的联系呢?
骨折,即骨骼结构的断裂,是临床中极为常见的损伤类型。尽管现代医学在骨折治疗方面已经取得了显著的进步,但仍面临着诸多挑战。
目前,骨折的治疗方法主要包括保守治疗和手术治疗。保守治疗通常适用于轻微骨折,通过固定、制动和康复锻炼等手段促进骨折愈合。然而,保守治疗存在固定时间长、易导致关节僵硬和肌肉萎缩等缺点。此外,若骨折存在错位情况,保守治疗可能形成畸形愈合,影响正常功能。手术治疗则适用于严重骨折或错位骨折,通过内固定或外固定等手段恢复骨骼结构。但手术本身具有风险,可能引发出血、感染、神经损伤等并发症,且术后康复也存在一定困难。
骨折愈合的过程复杂且漫长,受多种因素影响。一般来说,轻微骨折可能需要数周到数月恢复正常,而严重骨折则可能需要更长时间。此外,骨折部位、治疗方式、患者年龄和健康状况等也会影响骨折愈合的速度和质量。例如,手部骨折可能数周恢复,而腿部骨折则可能需要数月甚至更长时间。对于老年患者或身体状况较差的患者,骨折愈合的速度和质量往往更差。
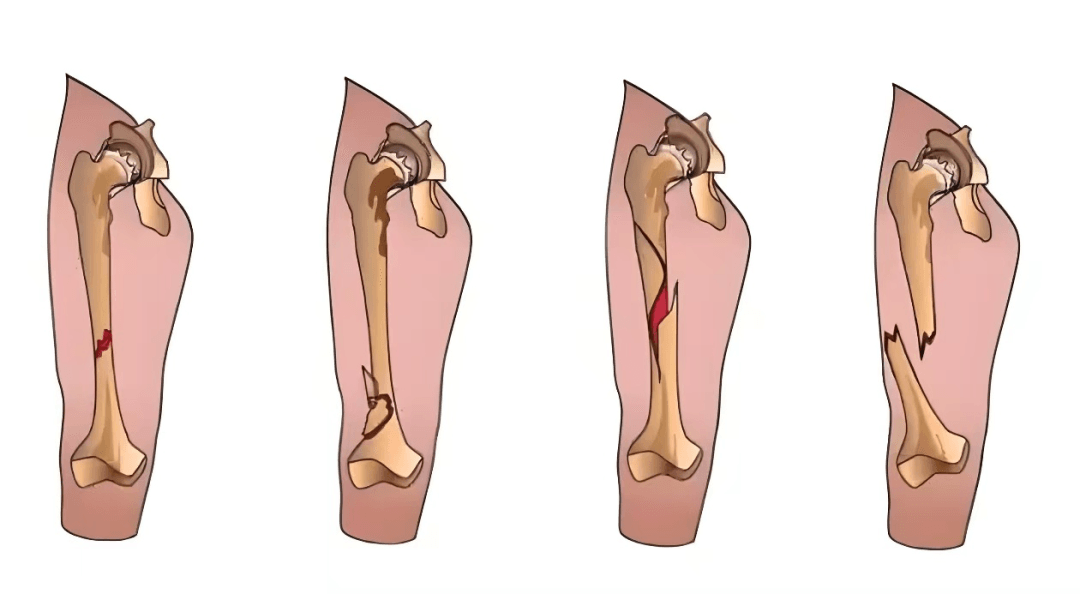
值得注意的是,骨折还可能引发创伤性大器官损伤。当骨折经治疗后在超过同类骨折正常愈合所需时间仍未达到完全愈合标准时,称为骨折延迟愈合。其临床表现包括局部肿胀、压痛、叩击痛阳性、异常活动、功能障碍等。骨折延迟愈合的原因有很多,如创伤过重、骨折部位血液供应破坏、感染、固定不牢以及过早负重等。因此,骨折治疗需要综合考虑多种因素,进行个体化评估和决策。
外泌体与骨折愈合联系
据统计,约有 10% 的骨折患者会面临愈合不佳的困境。这一现象背后,是骨折愈合所涉及的两个关键阶段在起着主导作用。首先是合成代谢组织膨胀期,在这个阶段,身体像是一位积极的建设者,努力地为骨折修复奠定基础,各种营养物质和细胞因子聚集到骨折部位,促进新组织的生成与生长,让受伤的部位开始初步的修复与重建工作。紧接着是分解代谢组织重塑期,此时身体如同一位精细的雕塑家,对新生组织进行雕琢与塑形,去除不必要的部分,使骨骼结构逐渐恢复到接近受伤前的状态,并且在强度和功能上也不断优化。
这两个关键阶段并非独立运作,它们受到多种因素的共同调控。干细胞活性在其中扮演着极为重要的角色。干细胞就像是一群万能的工匠,它们具有分化成各种细胞类型的潜力,可以转化为成骨细胞,直接参与新骨的形成;也能够分化为软骨细胞,构建软骨组织,为骨折部位提供临时的支撑与缓冲,并且随着愈合进程的推进,还能进一步促进软骨向骨组织的转化。在骨折的生物药理学治疗领域,局部应用(如骨形态发生蛋白BMP)和全身性治疗(如甲状旁腺素PTH)是两种主要策略。然而,近年来,外来体疗法作为一种新兴的替代疗法,正逐渐展现出其在骨折愈合方面的巨大潜力。这种疗法主要利用骨髓来源的间充质干细胞(MSC)作为细胞供应者,通过分泌外来体(即外泌体)来促进骨折愈合。
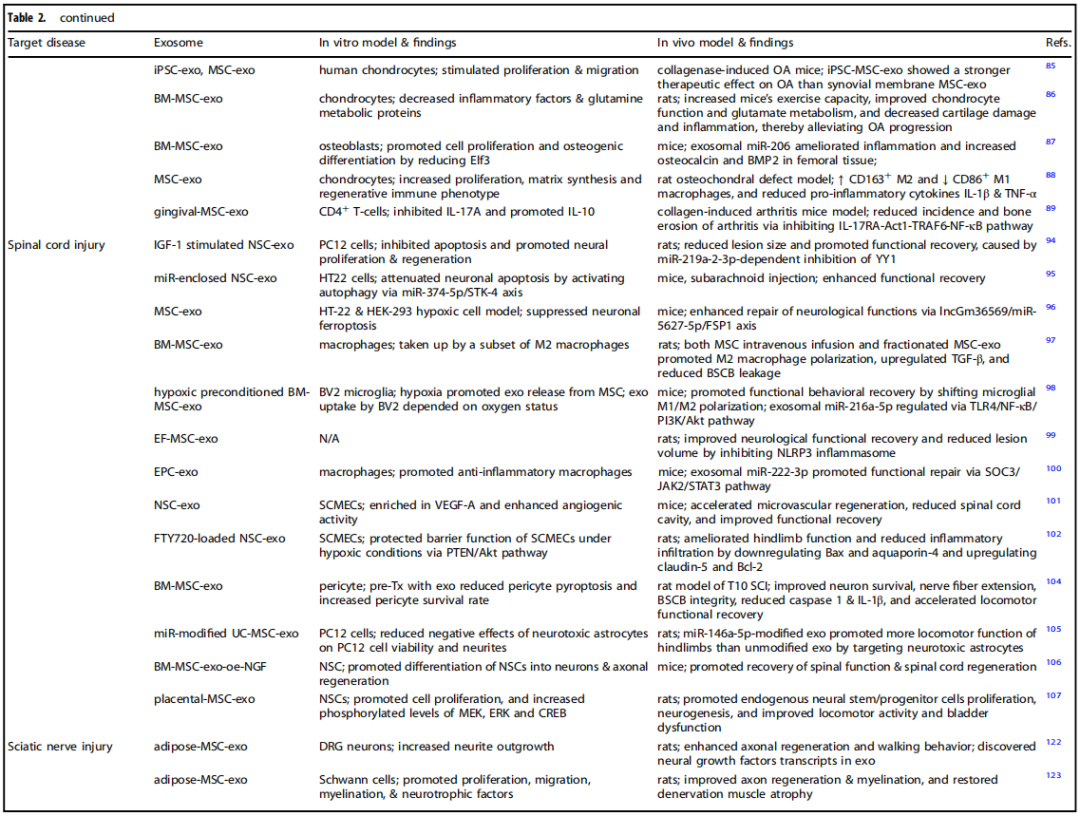
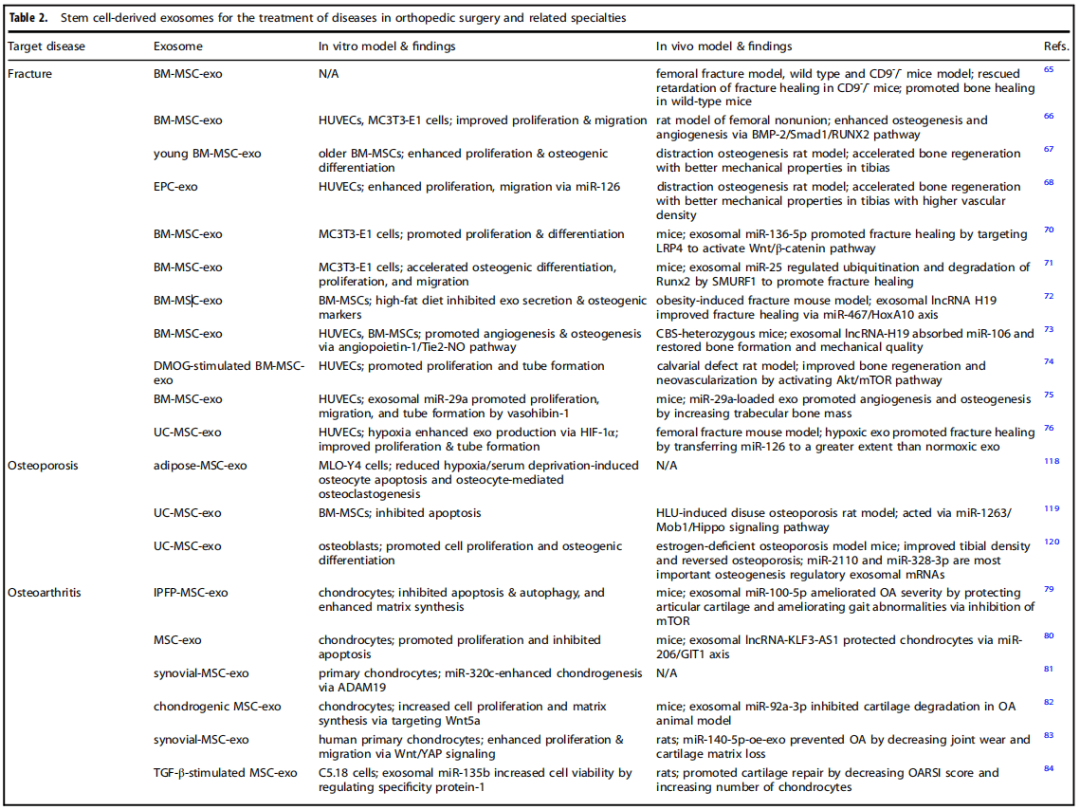
图:干细胞来源的外泌体用于治疗骨科手术和相关专业的疾病
早期的研究借助构建多样化的骨折愈合动物模型,有力地证实了外泌体在骨折愈合过程中所发挥的积极作用。在股骨干横向骨折模型中,外泌体不仅显著加速了野生型小鼠的骨生成,还有效挽救了因CD9−/−基因缺陷而导致骨愈合能力低下的CD9−/−小鼠的骨折愈合延迟现象。在股骨骨不连模型中,外泌体通过激活BMP2/Smad1/RUNX2等一系列信号通路,有效促进了骨生成和血管生成,从而显著加速了骨折的愈合进程。此外,在胫骨牵张成骨模型中,年轻骨髓间充质干细胞分泌的外泌体被证实能够显著提升老年骨髓间充质干细胞的成骨潜能,并有力促进了老年大鼠的新骨形成。同时,内皮祖细胞(EPC)衍生的外泌体也被发现能够通过强烈刺激血管生成,在牵张成骨过程中进一步加速骨组织的再生。
外泌体中的RNA成分,尤其是microRNA(miRNA)和长链非编码RNA(lncRNA),是调节受体细胞基因表达和表型功能的关键性分子。研究揭示,骨髓间充质干细胞(MSC)来源的外泌体中的miR-136-5p能够通过Wnt/β-catenin信号途径抑制下游靶基因LRP4的表达,从而在体外环境中有效促进成骨细胞的增殖和分化。而MSC来源的外泌体中的miR-25则能够通过精细调控SMURF1和Runx2的泛素化及降解过程,显著促进小鼠的骨折愈合。此外,骨特异性lncRNA H19也被发现能够在肥胖诱导的骨折模型中有效逆转高脂饮食对成骨分化和骨折愈合产生的负面影响,并通过miR-467/HoxA10轴发挥重要的保护作用。在免疫受损的裸鼠模型中,外泌体lncRNA H19还被证实能够显著改善骨生成和血管生成,其机制涉及血管生成素1/Tie2-NO信号通路的激活。
应用前景
外泌体在骨折治疗中的巨大潜力已经引起了广泛关注。作为天然的药物递送生物载体,外泌体具有多种优势,如低毒性、高生物相容性和易于制备等。以下将探讨外泌体在骨折治疗中的具体应用前景。
作为药物递送生物载体
外泌体作为一种天然的药物递送生物载体,在骨折治疗中展现出巨大潜力。它可以通过包裹药物或基因治疗物质等实现精准给药,提高药物的生物利用度和靶向性。同时,外泌体还具有免疫逃逸功能,能够避免被免疫系统识别和清除。因此,外泌体在骨折治疗中可以作为一种有效的药物递送系统,促进骨折愈合。
例如,南京医科大学的研究表明,低氧预处理的外泌体能够通过激活HIF-1α介导miR-126的产生,进而促进骨折愈合。这一研究为外泌体在骨折治疗中的应用提供了新的思路。通过优化外泌体的制备方法和给药途径等,可以进一步提高其治疗效果和安全性。
作为干细胞治疗的补充和替代
干细胞疗法在骨折治疗中已经取得了一定的成果,但干细胞的使用也面临着一些挑战,如细胞来源有限、免疫排斥和伦理问题等。外泌体作为干细胞分泌的微小囊泡,具有与干细胞相似的生物学功能,但不存在上述挑战。因此,外泌体可以作为一种干细胞治疗的补充和替代方法,用于促进骨折愈合。通过提取和纯化干细胞分泌的外泌体,可以将其用于治疗骨折患者。外泌体中的多种生物活性成分,如蛋白质、脂质和微小RNA等,可以作用于骨折部位的细胞,促进血管生成、骨组织再生和免疫调节等过程,从而加速骨折愈合。
结论与展望
综上所述,外泌体在骨折治疗中具有巨大的潜力。作为天然的药物递送生物载体和细胞间通讯的重要媒介,外泌体能够通过多种机制促进骨折愈合。未来,需要进一步研究外泌体的作用机制和临床应用,以更好地服务于患者。未来的研究还应关注外泌体与其他治疗方法的联合应用,如与生物材料、生长因子或基因治疗等结合,以进一步提高骨折治疗的效果和安全性。通过跨学科的合作和创新,我们有理由相信,外泌体将会为骨折治疗领域带来革命性的突破。
参考文献
Tan, F, Li, X, Wang, Z. et al. Clinical applications of stem cell-derived exosomes. Sig Transduct Target Ther 9, 17 (2024).
免责声明:本文旨在科普相关知识,不作为医疗指导意见。
编辑|Ning.ZG
审核|Geng.ZG

