
干细胞,作为一群拥有自我更新与功能组织重建独特能力的未分化细胞,近年来在再生医学领域展现出了巨大的应用潜力。尽管干细胞疗法在特定疾病的管理上已表现出显著优势,甚至在某些情况下优于传统手术,但其临床转化仍面临诸多挑战,包括潜在的缺点和限制。在此背景下,干细胞来源的外泌体因其多重优势而备受关注。这些外泌体不仅无免疫原性、无输注毒性,还易于获取与保存,同时不具备致瘤潜力和伦理问题。更重要的是,它们能够继承其亲本干细胞(如胚胎干细胞和成体干细胞)的多能性,并通过垂直递送机制实现类似的治疗效果。这一特性为未来的疾病治疗提供了全新的思路和方法。
干细胞外泌体的基础特性
外泌体(exosomes)是细胞分泌的膜性囊泡,直径仅为30-150纳米。这些微小囊泡虽然体积微小,但却携带着丰富的生物活性物质,如蛋白质、脂质和核酸。这些物质能够与损伤细胞进行“交流”,调节细胞功能,并发挥抗炎、免疫调节和组织修复的作用。外泌体广泛存在于各种体液中,包括血液、淋巴液、脑脊液、唾液、尿液和羊水等。
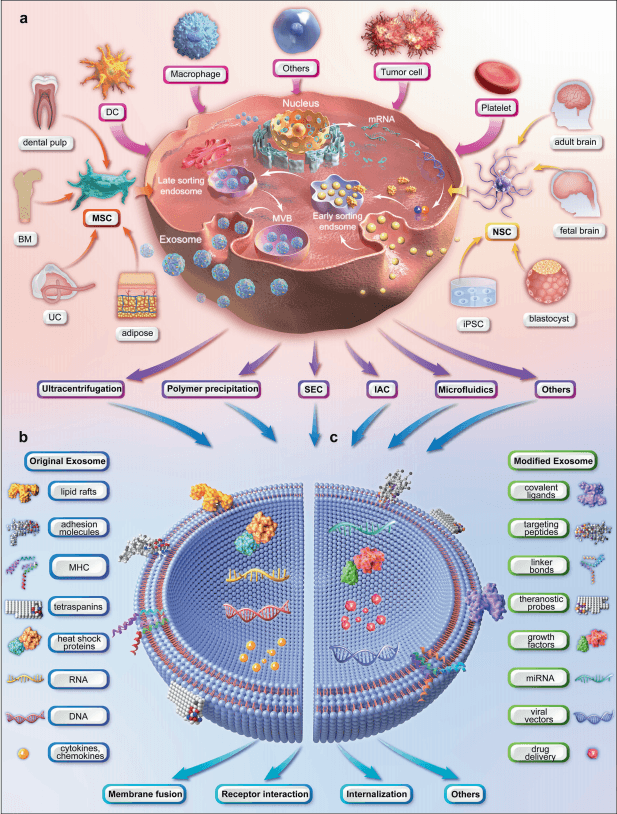
图1:a.外泌体的产生和纯化(MSC和NSC用作多能干细胞的实例)b.天然外泌体的含量c.外来体的修饰。(BM骨髓、DC树突状细胞、IAC免疫亲和层析、iPSC诱导的多能干细胞、MHC主要组织相容性复合物、miRNA、microRNA、MSC间充质干细胞、MVB多泡体、NSC神经干细胞、SEC尺寸排阻层析、UC脐带)
干细胞外泌体具有类似于干细胞的生物学功能,同时兼具体积小、易穿透生物膜、低免疫原性、易存储等优点。外泌体通过转运多种生物活性成分,参与了机体的生理病理过程,具有在一定程度上体现来源细胞的生理病理状态、信息传递、清除细胞内成分及充当药物载体等生物学功能。
间充质干细胞(MSCs)来源的外泌体因其低免疫原性和高安全性,在治疗过程中尤为引人注目。它们不包含活细胞,因此避免了细胞移植可能带来的免疫排斥风险。此外,外泌体的生物相容性好,易于制备和存储,为多种疾病的治疗提供了新的可能。
干细胞外泌体的治疗机制
来源于干细胞的外泌体(例如,胚胎干细胞、诱导多能干细胞、造血干细胞、间充质干细胞、神经干细胞和内皮干细胞)能够治疗整形外科、神经外科、普通外科、心胸外科、泌尿外科、头颈外科、眼科和妇产科中遇到的多种疾病。干细胞来源的外泌体的不同治疗作用是通过组织特异性反应和细胞特异性分子信号传导途径的分级调控来实现的。
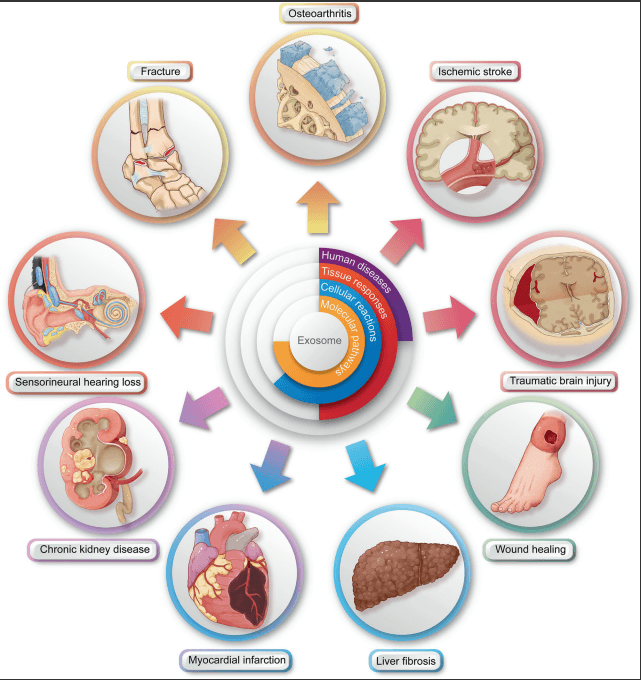
图2.外泌体的治疗作用是通过疾病特异性组织反应、组织特异性细胞改变和细胞特异性分子信号传导途径的分级调控
疾病特异性组织反应
在疾病状态下,特定组织中的细胞会分泌具有特定组成的外泌体,这些外泌体能够识别并结合到疾病相关的受体细胞上,从而引发一系列的组织反应。这种反应具有疾病特异性,即不同疾病状态下分泌的外泌体组成不同,所引发的组织反应也不同。
组织特异性细胞改变
外泌体与受体细胞结合后,会通过多种机制影响受体细胞的功能和状态。这些机制包括但不限于
外泌体表面蛋白与受体结合:外泌体表面的蛋白可以与受体细胞的表面受体结合,从而调控下游信号转导途径,影响细胞的增殖、分化、凋亡等过程。
外泌体与细胞膜融合:外泌体可以与受体细胞的细胞膜融合,将其携带的功能性内容物(如转录因子、调节性RNA等)导入受体细胞内部,直接调控受体细胞的基因表达和生物学行为。
受体细胞内吞外泌体:受体细胞还可以通过胞饮或吞噬作用将外泌体整个吸收进细胞内,外泌体在细胞内释放其内容物,进一步影响细胞的功能和状态。
这些机制导致组织特异性细胞发生改变,从而实现对疾病的干预和治疗。
细胞特异性分子信号传导
外泌体携带的生物信息分子在受体细胞内释放后,会参与细胞内的信号传导途径,进而影响细胞的生物学行为。这种信号传导途径具有细胞特异性,即不同类型的细胞对外泌体携带的生物信息分子的响应方式和程度不同。此外,这种信号传导途径还呈现分级调控的特点,即外泌体携带的生物信息分子可以通过调控多个下游信号分子和通路,形成复杂的信号网络,实现对细胞功能的精细调控。
干细胞外泌体在外科治疗中的应用
促进组织修复与再生
干细胞外泌体中含有多种生物活性物质,如生长因子、细胞因子等,这些物质在促进损伤组织的修复和再生方面发挥着重要作用。在外科手术中,组织损伤是不可避免的,而干细胞外泌体能够提供必要的营养和支持,加速组织修复过程。例如,在急性肝损伤(ALI)和肝纤维化治疗中,间充质干细胞(MSC)衍生的外泌体可以通过特定的机制改善肝功能,减少肝损伤。
抗炎作用
干细胞外泌体还具有显著的抗炎作用,能够减轻炎症反应,降低炎症因子水平。这对于外科手术后预防感染、减轻术后疼痛等方面具有重要意义。在类风湿性关节炎、肺部疾病等炎症性疾病的治疗中,干细胞外泌体显示出良好的治疗效果。
抗氧化作用
干细胞外泌体能够清除体内的自由基,减轻氧化应激,保护细胞免受损伤。在抗氧化治疗、抗衰老等领域,干细胞外泌体具有广泛的应用前景。例如,在皮肤外科治疗中,干细胞外泌体可以促进皮肤损伤的修复,减轻炎症反应,并有助于减少皱纹和细纹,改善皮肤纹理。
具体疾病治疗
急性肝损伤与肝纤维化:
急性肝损伤:间充质干细胞衍生的外泌体可通过稳定相关分子机制防止铁变态反应,或通过外泌体中的特定miRNA改善由IL-6诱导的肝损伤。
肝纤维化:源自三维人ESC球体的外泌体可通过使Smad通路失活,减弱肝星状细胞的活化并抑制肝纤维化。
急性胰腺炎:
iPSC衍生的间充质干细胞外泌体可通过特定通路改善重症急性胰腺炎引起的心肌损伤。
血管疾病:
胎盘间充质干细胞衍生的外泌体输注可促进血管生成。
造血干细胞衍生的外泌体可修复小鼠缺血的后肢。
人类iPSC衍生的外泌体通过外泌体miRNA显示新血管生成效应。
EPC衍生的外泌体可通过增强内皮细胞功能促进血管修复并加速血管再内皮化,对球囊损伤具有保护作用。
坏死性小肠结肠炎:
源自羊水MSC、骨髓MSC、羊水NSC和新生儿肠NSC的外泌体可以降低实验性NEC的发生率和严重程度。
脓毒症:
EPC衍生的外泌体可以改善脓毒症结局,减少肺和肾血管渗漏、改善器官功能并提高存活率。
皮肤疾病:
干细胞外泌体可以促进皮肤损伤的修复,减轻炎症反应,加速伤口愈合,降低疤痕形成的风险。例如,在烧伤、烫伤等皮肤损伤的治疗中,干细胞外泌体具有显著的治疗效果。
其他应用
肿瘤治疗:研究发现,干细胞外泌体可以通过调节肿瘤细胞的生长、凋亡等过程,抑制肿瘤的生长和转移。这为肿瘤治疗提供了新的思路。
自身免疫性疾病治疗:MSC来源的外泌体能够复制MSC的功能,克服传统细胞治疗的局限性,对多发性硬化症、系统性红斑狼疮、Ⅰ型糖尿病、类风湿性关节炎等在内的自身免疫性疾病治疗也取得了实质性进展。
未来展望
干细胞来源的外泌体,作为干细胞疗法的创新替代方案,在外科治疗领域已经彰显了巨大的发展潜力。随着科研探索的不断深入和技术水平的持续提升,其应用前景正逐步拓展至更广阔的医疗范畴。然而,当前仍面临一些亟待解决的难题,包括外泌体产量不足、提取效率低下,以及分离纯化技术的进一步精进。为此,未来的研究与实践将致力于不断优化制备与纯化工艺,力求大幅提升外泌体的产量与纯度,并集中力量对整个治疗流程的各个关键环节进行深度优化与升级,以期在外科治疗中实现更为广泛且高效的应用。
参考文献
【1】Tan, F, Li, X, Wang, Z. et al. Clinical applications of stem cell-derived exosomes. Sig Transduct Target Ther 9, 17 (2024).
【2】Wu, Y., Cao, Y., Chen, L. et al. Role of Exosomes in Cancer and Aptamer-Modified Exosomes as a Promising Platform for Cancer Targeted Therapy. Biol Proced Online 26, 15 (2024).
免责声明:本文旨在科普相关知识,不作为医疗指导意见。
编辑|Ning.ZG
审核|Geng.ZG

