
创伤性脑损伤(TBI)作为全球范围内的重大疾病,其发病率居高不下。据估算,全球每年有5000万至6000万人遭受TBI,且半数以上人群在一生中至少经历一次TBI。这一状况不仅导致高达4000亿美元的经济损失,还成为年轻人死亡和致残的主要原因,特别是在中低收入国家。
在中国,TBI的发生率同样呈上升趋势,截至2017年底,已有约1.39亿人次遭受过TBI,占全国人口的18%,对社会经济及家庭造成了沉重负担。
舒马赫的奇迹人生
迈克尔·舒马赫,这位昔日的赛车传奇,曾七度夺得一级方程式世界冠军,他的名字与速度、巅峰和不断挑战极限紧密相连。然而,2013年的一次滑雪意外却彻底改变了他的人生轨迹。

在法国阿尔卑斯山滑雪时,舒马赫不慎摔倒,头部右侧猛烈撞击岩石,头盔瞬间破裂。尽管他最初意识尚存,但已无法连贯回答问题,行为异常,随后陷入深度昏迷。这次意外让他远离了熟悉的赛道和热情的粉丝,身体健康也遭受了巨大挑战,肌肉萎缩、骨骼退化,身高缩减至1.6米,体重更是暴跌至90斤。在昏迷的五年间,他接受了无数次脑部手术,并尝试了当时颇具创新性的干细胞治疗。
据法国《巴黎人报》报道,舒马赫在接受干细胞治疗后,健康状况取得了显著进展。一位参与治疗的医护人员透露:“他确实是我的病人,我可以肯定地说,他是有意识的。”干细胞治疗的有效性在多个医学研究中已得到验证。
在家人和医疗团队的精心呵护下,舒马赫逐渐从昏迷中苏醒,虽然语言交流仍存在一定困难,但整体状况已大为好转。十一年后的今天,他首次公开露面,参加了女儿的婚礼。舒马赫的案例不仅彰显了干细胞治疗的现实价值和未来潜力,更为那些在传统治疗中陷入困境的患者带来了新的希望。
TBI的传统与新兴治疗方法
治疗TBI的传统方法主要包括药物治疗、手术治疗和康复治疗。药物治疗虽然能在初期减轻脑水肿和颅内压,但效果有限且可能伴随副作用;手术治疗虽然能直接清除血肿、修复骨折,但存在感染、出血等风险,且术后恢复过程漫长;康复治疗则通过物理、语言、心理等多种手段帮助恢复受损功能,但疗效因个体差异而异。
近年来,干细胞治疗凭借其自我更新、多向分化潜能以及分泌神经营养因子、免疫调节功能等独特生物学特性,为TBI治疗开辟了新的道路。
干细胞治疗创伤性脑损伤的机理
干细胞治疗在创伤性脑损伤中展现出巨大潜力的关键在于其多种生物学特性。
细胞再生与修复:干细胞具有自我复制和分化的能力,能够在体内外环境中转化为多种类型的细胞,如神经元、星形胶质细胞、少突胶质细胞等。当脑部受损时,干细胞能够迁移到受损区域,通过分裂增殖产生新的神经细胞来替代受损或死亡的神经元,从而促进神经组织的再生与修复。
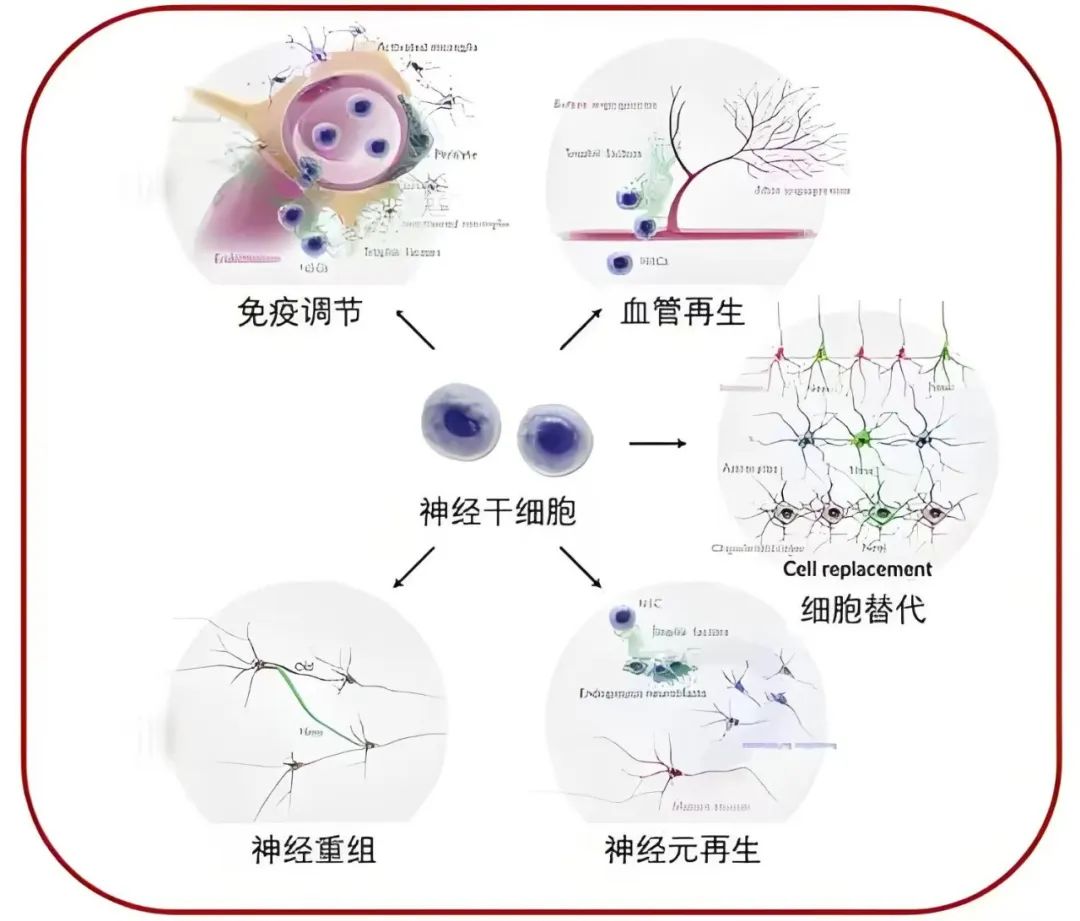
神经营养因子分泌:干细胞能够分泌多种神经营养因子,如神经生长因子(NGF)、脑源性神经营养因子(BDNF)等,这些因子对神经元的存活、生长和修复至关重要。它们能够刺激受损神经元的再生,促进轴突延伸,重建神经网络,从而改善受损区域的功能。
免疫调节功能:间充质干细胞等类型的干细胞具有免疫调节特性。它们能够减轻神经炎症,减少炎症细胞的浸润和炎症介质的产生,从而保护神经组织免受进一步损伤。同时,这些细胞还能分泌抗炎因子,如IL-10、TGF-β等,抑制炎症反应,有助于恢复正常的免疫微环境。
血管生成与血脑屏障修复:干细胞移植能够促进血管生成,为受损区域提供充足的血液供应,有助于神经组织的恢复。此外,干细胞还能修复受损的血脑屏障,维持脑内环境的稳定。
神经保护与支持:干细胞能够为存活的神经元提供支持,通过形成神经支架来稳定并维持其功能。同时,它们还能提供细胞外基质,为新生神经元的生长和分化提供必要的环境。
刺激神经重塑:脑外伤后,大脑可能会经历神经可塑性变化,即神经网络的重新配置。干细胞可能通过参与这一过程来帮助受损区域的神经网络重构,提高受伤神经元的连接性和功能性。
hucms对创伤性脑损伤大鼠模型治疗效果
不同途径移植人脐带间充质干细胞对创伤性脑损伤大鼠模型治疗效果的影响。实验采用改良的Feeney自由落体撞击法制备TBI大鼠模型,并通过不同途径移植人脐带间充质干细胞(hUCMSCs)探讨其治疗效果。
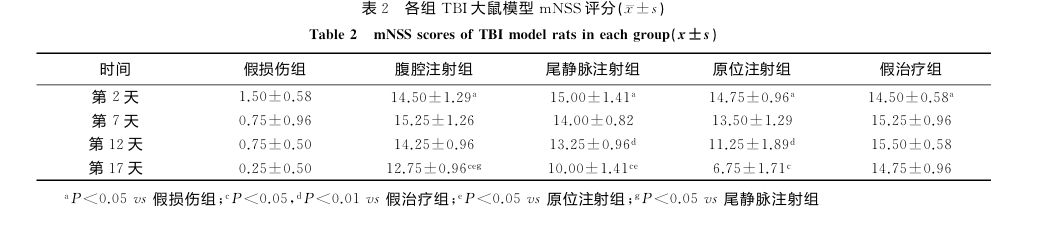
研究方法:采用腺病毒-绿荧光蛋白转染标记大鼠,并通过改良的自由落体撞击法制备TBI模型。将模型大鼠分为假损伤组、腹腔注射组、尾静脉注射组、原位注射组和假治疗组。通过改良神经功能缺损评分(mNSS)对各组模型动物的治疗效果进行评价。同时,利用冰冻切片荧光显微镜检测移植人脐带间充质干细胞(hUCMSC)在各组动物体内的归巢效率。
研究结果:Ad-GFP转染后,超过90%的hUCMSC表达了GFP蛋白。mNSS评分结果显示,hUCMSC移植治疗中,原位注射组的治疗效果最佳(P<0.05),其次为尾静脉注射组(P<0.05),但TBI大鼠模型的神经功能并未完全恢复。在冰冻切片荧光显微镜下观察大鼠脑部损伤部位发现,原位注射组的hUCMSC归巢数量最多。
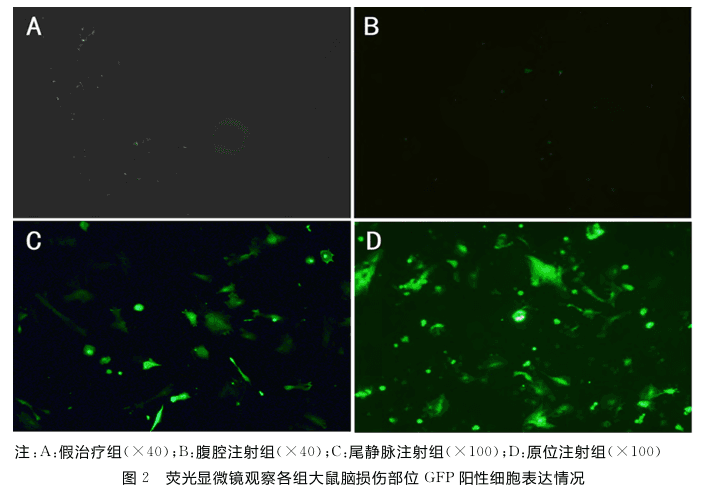
结论:人脐带间充质干细胞移植对TBI大鼠模型具有治疗作用,且最佳的治疗途径是原位注射。
结论
干细胞治疗因其独特的生物学特性,为TBI的治疗提供了新希望。通过细胞再生与修复、分泌神经营养因子、免疫调节、血管生成与血脑屏障修复、神经保护与支持以及刺激神经重塑等机理,干细胞能够显著改善TBI患者的健康状况。未来,随着干细胞治疗技术的不断发展和完善,相信将有更多患者从中受益,为TBI的治疗开辟新的篇章。
参考文献
[1] 王晓辉,杨志华,谢艳芳,等.不同途径移植人脐带间充质干细胞对创伤性脑损伤大鼠的治疗效果[J].西北国防医学杂志,2020,41(08):483-488.
[2] 高洋,秦合伟,刘丹丹.间充质干细胞调控免疫反应治疗创伤性脑损伤的作用机制研究进展[J/OL].解放军医学杂志,1-13[2024-11-28].
[3]亓立峰.脐带间充质干细胞及细胞因子共移植治疗脑损伤的分子机理研究[D].山东大学,2018.
免责声明:本文旨在科普相关知识,不作为医疗指导意见。
编辑|Lin.ZG
审核|Geng.ZG

