
2025年4月25日,斯坦福大学Edgar G. Engleman团队在Science 在线发表题为“Tumor-derived erythropoietin acts as an immunosuppressive switch in cancer immunity”的研究论文,为了探究治疗失败的原因,该研究检测了自发性的小鼠肝细胞癌(HCC)模型,这些模型分别具有富含炎症性 T 细胞的肿瘤微环境或缺乏炎症性 T 细胞的肿瘤微环境(TME)。

免疫耐受是一种对通常预期会激发免疫反应的物质漠不关心或无反应的状态,在移植和自身免疫性疾病中是有益的,但在癌症中是有害的。cDC1s是一种典型的抗原提呈细胞,它通过吞噬凋亡细胞或吞噬坏死细胞来诱导相应的细胞相关抗原特异性T细胞免疫反应,从而专门获取细胞相关抗原。由于其独特的将细胞相关抗原交叉呈递到CD8+ T细胞的能力,cDC1s是对抗肿瘤和病毒感染的免疫所必需的。
该研究由Edgar G. Engleman教授与张香月博士共同领衔,深入揭示了1型传统树突状细胞(cDC1s)在免疫激活与免疫耐受之间做出选择的核心机制。
cDC1s作为一种关键的抗原提呈细胞,具有独特的交叉呈递能力,能够将细胞来源的抗原呈递给CD8+ T细胞,在抗肿瘤和抗病毒免疫中发挥着不可替代的作用。然而,cDC1s如何在免疫激活与免疫耐受之间进行精准调控,一直是免疫学领域的未解之谜。Engleman团队的研究发现,促红细胞生成素受体(EPOR)在cDC1s的功能抉择中扮演了关键开关的角色。
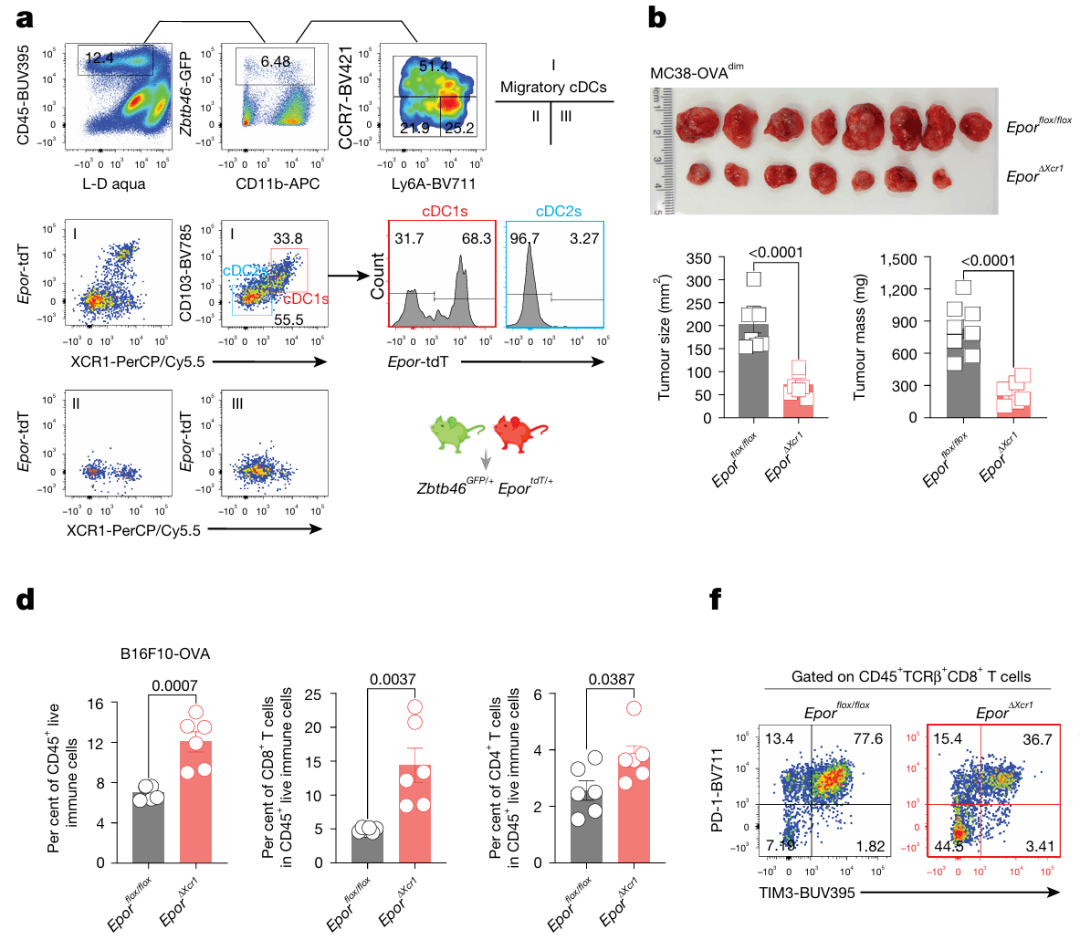
研究表明,cDC1s表面的EPOR表达水平直接决定了其耐受性功能和抗原特异性T细胞反应的阈值。当EPOR信号通路被激活时,cDC1s会向免疫耐受型转化,诱导抗原特异性T细胞产生免疫耐受;而当EPOR信号被阻断时,cDC1s的免疫原性会显著增强,能够有效激活T细胞免疫反应。具体而言,EPOR的缺失会导致cDC1s中参与MHC I类和II类介导的抗原呈递、交叉呈递以及共刺激的基因表达上调,促进cDC1s的免疫原性成熟。
在肿瘤免疫方面,cDC1s的EPOR缺陷能够显著增强抗肿瘤T细胞免疫,具体表现为肿瘤引流淋巴结中前体耗尽肿瘤抗原特异性CD8+ T细胞的产生增加,且这些T细胞能够在肿瘤内有效维持,同时肿瘤内调节性T细胞(Treg细胞)的数量减少,最终抑制肿瘤生长。这一发现不仅深化了对树突状细胞免疫调控机制的理解,更为肿瘤免疫治疗提供了新的干预靶点。
此外,该研究的意义还延伸到了自身免疫病和器官移植领域。免疫耐受在自身免疫病中有助于防止免疫系统攻击自身组织,在器官移植中则能减少排斥反应的发生。通过靶向cDC1s上的EPOR,研究人员可以精准调控T细胞免疫耐受的状态,为自身免疫病的治疗和器官移植后的免疫抑制提供全新的策略
2025年12月10日,斯坦福大学Edgar G. Engleman及张香月共同通讯在《Nature》在线发表题为“Erythropoietin receptor on cDC1s dictates immune tolerance”的研究论文,该研究表明促红细胞生成素受体(EPOR)作为一个关键开关,决定了cDC1s的耐受性功能和抗原特异性T细胞反应的阈值。靶向cDC1s上的EPOR诱导或抑制T细胞免疫耐受可能具有治疗多种疾病的潜力
研究团队通过对自发性小鼠肝细胞癌模型的深入研究发现,肿瘤细胞会自主分泌促红细胞生成素(EPO),而这一分泌行为直接决定了肿瘤的免疫类型。肿瘤衍生的EPO会与肿瘤相关巨噬细胞(TAMs)表面的促红细胞生成素受体(EPOR)特异性结合,触发一系列信号传导通路,最终促使TAMs向免疫调节型转化。在这一过程中,NRF2介导的EPO耗竭发挥了关键作用,使得TAMs能够主动营造出一个无炎症的肿瘤微环境(TME)。在这种环境下,抗肿瘤T细胞的活化与增殖受到显著抑制,肿瘤得以顺利逃脱免疫系统的监视与清除。
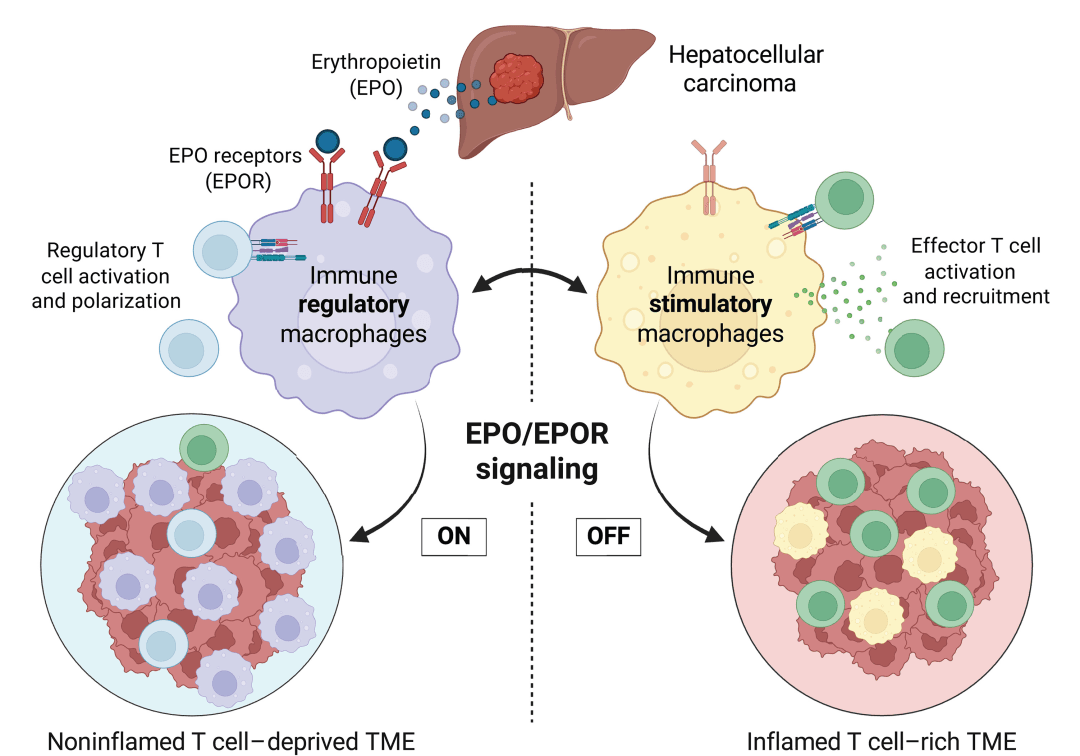
更为重要的是,研究团队通过实验证实,无论是去除肿瘤细胞分泌EPO的能力,还是阻断TAMs表面的EPOR,都能显著改变肿瘤微环境的性质,使其从无炎症状态转变为炎症状态,进而激发强大的抗肿瘤T细胞免疫反应,最终实现肿瘤的消退,且这一效果与肿瘤的基因型无关。这一发现明确了EPO/EPOR轴作为抗肿瘤免疫的免疫抑制开关的核心作用,为“冷肿瘤”的治疗提供了精准靶点。
进一步的临床数据分析显示,EPO水平升高与肝癌、肾癌、乳腺癌、结肠癌和皮肤癌等多种癌症患者的不良预后密切相关。这不仅验证了基础研究结果的临床相关性,更为后续的临床转化研究提供了有力依据。基于这一发现,研究团队已着手开发针对EPO/EPOR轴的新型癌症疗法,有望将“冷肿瘤”转化为对免疫治疗敏感的“热肿瘤”,为更多癌症患者带来希望。
Engleman团队的两项研究成果,在基础免疫学领域具有里程碑式的意义,它们不仅颠覆了人们对EPO功能的传统认知,将其从单纯的造血调控因子重新定义为免疫调控的核心开关,更揭示了EPO/EPOR轴在肿瘤免疫逃逸和树突状细胞介导的免疫耐受中的关键机制,为理解复杂的免疫调控网络提供了全新视角。
在临床转化方面,这些研究成果展现出了巨大的应用潜力。在肿瘤治疗领域,针对EPO/EPOR轴的靶向疗法有望成为免疫治疗的新方向。通过阻断EPO/EPOR信号通路,可以将“冷肿瘤”转化为“热肿瘤”,增强免疫检查点阻断疗法的疗效,为那些对现有免疫治疗不敏感的患者带来新的希望。此外,在CAR-T细胞治疗中,或许可以通过调控EPO/EPOR轴来增强CAR-T细胞的抗肿瘤活性和体内存活时间,进一步提升治疗效果。
在自身免疫病治疗中,通过靶向cDC1s上的EPOR诱导免疫耐受,可以有效抑制过度活化的自身免疫反应,为类风湿关节炎、系统性红斑狼疮等自身免疫病患者提供更加精准、安全的治疗方案。在器官移植领域,诱导免疫耐受能够减少长期使用免疫抑制剂带来的副作用,提高器官移植的成功率和患者的生活质量。
作用机制核心
cDC1-EPOR抑制剂特异性靶向cDC1细胞(经典1型树突细胞)上的促红细胞生成素受体(EPOR),抑制EPO-EPOR信号通路传导,从而逆转肿瘤诱导的免疫耐受,增强T细胞活化。
01信号通路阻断
抑制环节 生物学效应 免疫学结果
EPOR激活抑制 减少STAT3磷酸化 恢复抗原加工提呈能力
PD-L1表达下调 降低T细胞共抑制信号 增强CD8⁺T细胞活化
IL-10分泌减少 削弱免疫耐受微环境 逆转免疫抑制状态
02细胞功能恢复
抗原提呈修复:cDC1细胞作为交叉提呈肿瘤抗原的关键亚群,在抑制剂作用下,抗原提呈效率提升(实验数据:恢复至正常水平80%以上)。
T细胞激活增强:解除PD-L1等抑制信号,促进CD8⁺T细胞浸润和杀伤功能(联合PD-1抗体时协同增效)。
03整体治疗效应
单药效果:在动物模型中,恢复cDC1功能,打破肿瘤免疫逃逸屏障。
联合疗法优势:与PD-1抗体联用,通过双通路阻断(EPOR和PD-1),显著延长生存期(临床前数据:↑137%),形成协同抗肿瘤免疫。
结 语
斯坦福大学Edgar G. Engleman团队的两项研究,如同照亮免疫学黑暗角落的明灯,让我们看到了EPO/EPOR轴在免疫调控中的核心地位。从肿瘤免疫逃逸的“隐形开关”到免疫耐受的“核心调节器”,EPO/EPOR轴的多重功能被逐一揭开,为疾病治疗带来了前所未有的机遇。尽管从基础研究到临床应用还有漫长的道路要走,但这些发现无疑为我们指明了方向。未来,随着研究的不断深入,相信EPO/EPOR轴将在更多疾病的治疗中发挥关键作用,为人类健康事业做出重要贡献。
参考文献
1:Tumor-derived erythropoietin acts as an immunosuppressive switch in cancer immunity | Science
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

