
心力衰竭(心衰)是目前公共卫生面临的困境之一,其特点表现为高患病率、高死亡率、高住院率以及高花费,给患者及其家庭带来了难以承受的重负。
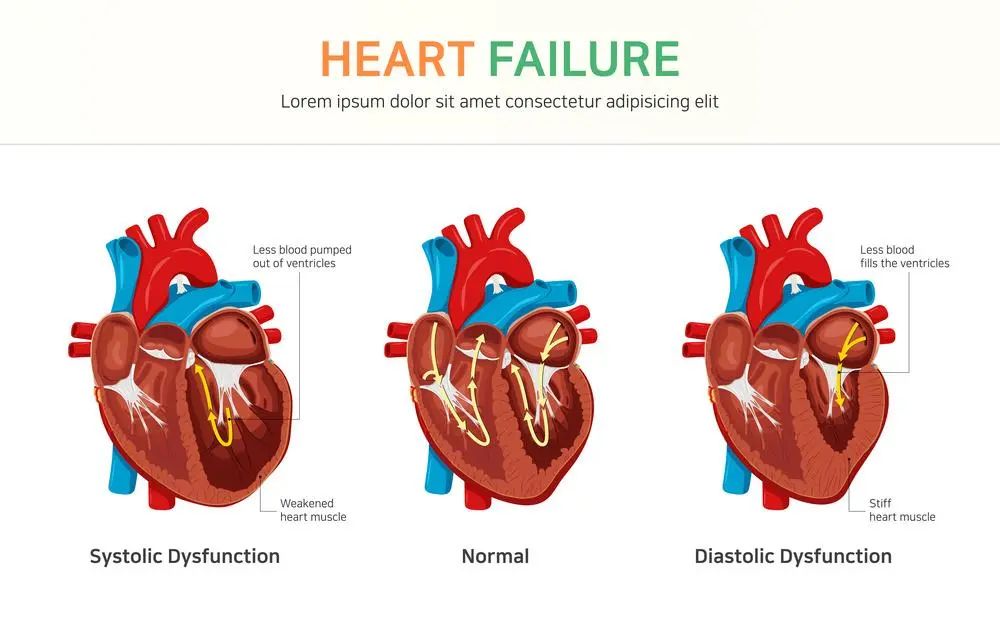
心力衰竭(Heart Failure, HF),简称心衰。是心血管疾病发展至中后期所呈现的一种极为严重的并发症,它源于心脏结构或功能的异常,构成了一个复杂的临床综合征。心衰的根源往往可追溯到患者早期未得到充分或及时干预的各种心脏疾病,这些疾病在时间的推移下逐渐恶化,最终步入心衰的终末阶段。
研究现状

根据最新发布的《中国心力衰竭诊断和治疗指南(2024)》及《中国心衰中心工作报告(2021)》中的权威数据,我们痛心地看到,仅35岁及以上的心衰患者人数就已激增至1,370万之巨,3年死亡率为28.2%,5年死亡率基本等同于一些常见的恶性肿瘤,心衰患者平均每年住院3.3次,平均每次因心衰住院的花费约39,064元,更令人担忧的是,每年新增的心衰患者数量将近300万,这一数字触目惊心,凸显了心衰问题的严峻性与紧迫性。

指南将心衰的四个阶段重新命名,并强调了高危人群预防心衰的重要性。
目前治疗策略
药物治疗
急性心衰的药物治疗
镇静剂:如吗啡等,用于使患者镇静,减轻心脏负担,同时扩张外周血管,减少回心血量。
血管扩张剂:如硝酸甘油、硝普钠等,通过扩张小静脉来降低回心血量,减轻心脏前负荷,缓解肺水肿。同时,这些药物还能扩张小动脉,降低外周阻力,减轻心脏后负荷。
正性肌力药物:如洋地黄类药物(地高辛等)和多巴酚丁胺等,通过增强心肌收缩力,改善心脏泵血功能,缓解心衰症状。。
利尿剂:如呋塞米、托拉塞米等,通过增加尿量,减轻体内液体潴留,降低心脏负荷。利尿剂是急性心衰治疗中改善症状的基石。
慢性心衰的药物治疗
ACEI或ARB类药物:如卡托普利、依那普利、氯沙坦、厄贝沙坦等,通过抑制肾素-血管紧张素系统,减轻心脏重构,延缓心衰进展。
β受体阻滞剂:如美托洛尔、比索洛尔等,通过减慢心率、降低心肌耗氧量,改善心脏功能,降低死亡率和住院率。
醛固酮受体拮抗剂:如螺内酯,通过拮抗醛固酮的作用,减少水钠潴留,降低心脏负荷,并具有一定的降低死亡率的作用。
缺点:由于心衰病理生理机制的极端复杂性,它跨越了多个层面,包括神经-内分泌系统的过度激活、代谢与炎症途径的失衡,以及细胞信号传导机制,导致心肌细胞的减少以及心室的重塑问题不能得到明显改善;治疗周期较长;药物的不良反应会对患者产生其他危害。
非药物治疗
生活方式干预
减少钠盐摄入:有助于减轻水肿,降低心脏负担。
戒烟限酒:改善心血管健康,减少心脏刺激。
适量运动:增强心肌功能,改善血液循环,但需在医生指导下进行。
体重管理:控制体重有助于减轻心脏负荷。
其他方式干预
体位引流:在白天采取头低脚高的姿势,夜间采取平卧位,每天至少保持一次。这种姿势有助于促进静脉回流,降低右心室压力,缓解呼吸困难的症状。
营养支持治疗:提供均衡饮食,必要时补充维生素B群和铁质等营养素。
心理护理:对患者进行心理咨询、给予正向情绪支持并营造温馨环境。良好的心理状态有利于患者配合医疗措施、提高生活质量。
限制液体摄入:建议每日饮水量不超过1500毫升,以减少体内液体潴留。
监测尿量:通过尿量变化评估体内水分平衡状态,及时调整液体摄入。
先进治疗方法
心脏再同步治疗(CRT):通过调整心脏收缩同步性来改善心功能。
起搏器植入(ICD):可预防恶性心律失常导致的心源性猝死。
心脏机械辅助装置治疗(LVAD):帮助心脏泵血,减轻心脏负担。适用于严重心脏事件后或准备行心脏移植术患者的短期过渡治疗以及急性心衰的辅助性治疗。
心脏收缩调节治疗(CCM):增强心肌收缩力。
迷走神经刺激治疗(VNS):调节自主神经功能,改善心脏功能。
脊髓刺激治疗(SCS):有助于缓解心衰症状。
缺点:非药物治疗方法并非适用于所有心衰患者。例如,心脏移植需要找到合适的供体心脏,且患者需符合一定的手术条件;费用高昂,部分非药物治疗方法如心脏移植、植入性心脏转复除颤器等,需要高昂的医疗费用;技术门槛高,需要先进的医疗技术和设备支持;术后可能出现排斥反应、感染等并发症;植入性心脏转复除颤器也可能出现误放电、电池耗尽等问题。
外泌体在HF中的发生作用
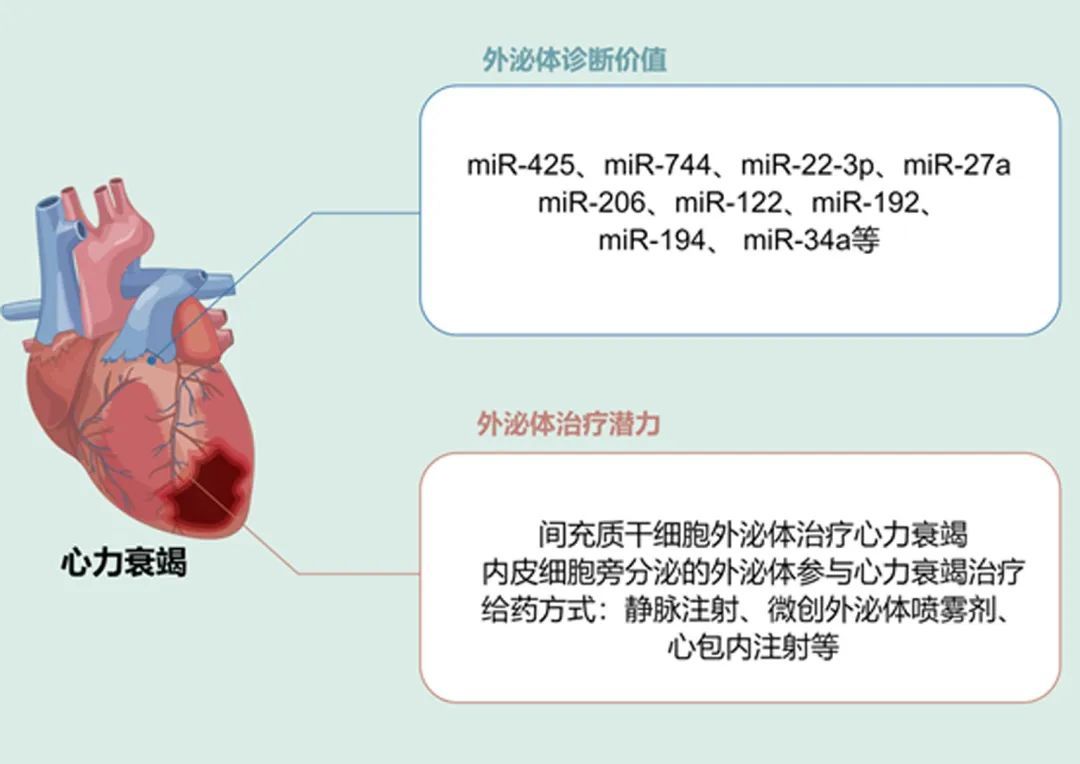
作为HF的诊断标志物
HF患者多种血清或血浆外泌体miRNA水平的改变能够在一定程度上反映心脏收缩、舒张功能以及心肌纤维化水平等,可以作为早期诊断HF的标志物。
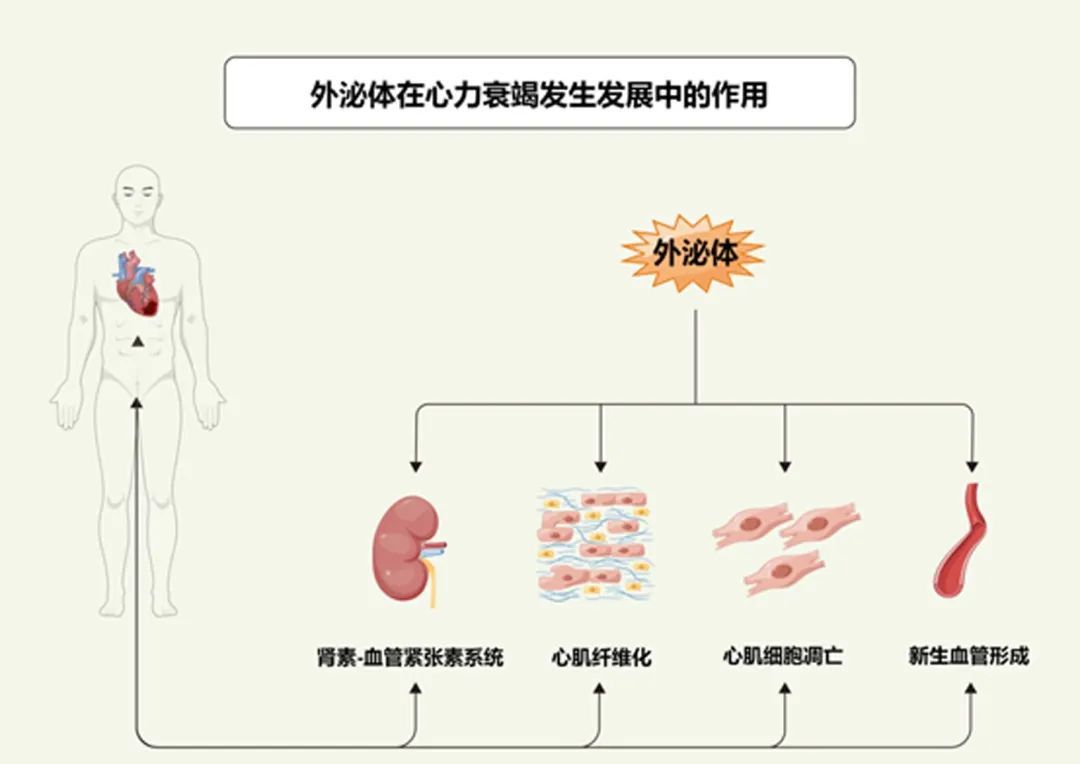
通过调节miRNA影响HF
外泌体在体内流动,通过调节某些microRNA (miRNA),调控各种信号机制,影响心脏细胞之间的相互交流。研究表明外泌体可以通过影响肾素-血管紧张素(renin-angiotensin system, RAS)系统、心肌纤维化、心肌细胞凋亡、新生血管形成等多方面参与HF的形成和发展。
Bang等发现沉默心脏成纤维细胞来源的外泌体miR-21-3p可引起山梨醇和含SH3结构域蛋白2和LIM结构域5表达水平上调,有助于减轻Ang Ⅱ诱发的心肌细胞肥大。此外,外泌体可能通过激活ACE2途径加速Ang Ⅱ向Ang 1-7的转化,下调ACE-Ang II-AT1R通路,助力RAS系统的平衡调节,从而改善心脏重构。
miR-21a-5p水平升高可以通过下调凋亡信号通路相关基因产物(如PTEN、Peli1和FasL)的表达来减少心肌细胞凋亡。外泌体miR-21-5p通过磷酸酶和Tensin同源物/Akt途径增强血管生成和心肌细胞存活能力,从而促进心脏修复。树突状细胞来源的外泌体miR-494-3p促进心肌梗死后的血管生成。
外泌体在心力衰竭治疗中的潜在应用
促进心脏修复
外泌体可以携带修复分子到达受损的心肌组织,促进心肌细胞的再生和修复。例如,干细胞衍生的外泌体已被证明可以通过抗炎反应、诱导血管生成、促进增殖和防止细胞凋亡等机制介导心脏组织修复。
改善心功能
研究表明,输注外泌体可能通过重新连接循环和外周器官中的内源性免疫细胞来发挥作用,以呈现修复表型。经过外泌体修饰的免疫细胞可以输送到心脏以实现组织修复,包括减轻炎症(心力衰竭的标志),从而改善心功能。
降低心衰事件发生率
临床试验显示,细胞疗法(包括使用外泌体)可能有助于降低心力衰竭患者的心衰事件发生率,提高患者的生活质量。
结论
外泌体在心血管疾病特别是心衰中发挥着多种重要作用。它们通过细胞间通讯、促进心肌细胞存活与再生、调控心脏纤维化与炎症以及血管生成与修复等机制参与心脏疾病的病理生理过程并为其治疗提供新的策略和方向。
免责声明:本文旨在科普相关知识,不作为医疗指导意见。
参考文献
[1]GUIDETTIF,ARRIGOM,FRANKM,etal.Treatment of advanced heartfailure-focus on transplantation and durable mechanical circulatory support:what does the future hold?[J].Heart Failure Clinics,2021,17(4):697-708.
[2]谢曼婷,谢冰冰,向秋玲.人诱导多能干细胞在扩张型心肌病模型建立及应用中的研究进展[J]医药卫生技.2024,45(09).
[3]Horie T, NishinoT,Baba O,KuwabaraY,Nakao T, Nishiga M,UsamiS, Izuhara M,Sowa N,Yaha gi N, Shimano H,MatsumuraS,InoueK,MarusawaH,NakamuraT,Hasegawa K,Kume N,Yokode M, Kita T, Kimura T,Ono K. MicroRNA-33 regulates sterol regulatory element-binding protein 1 expression in mice.Nat Commun.2013;4:2883.
编辑|Ning.ZG
审核|Geng.ZG

